题目内容
9.已知1~18号元素的离子aXm+、bY n+、cZP-、dWk-都具有相同的电子层结构,下列关系正确的是( )| A. | 若P>K,则还原性cZP-<dWk- | |
| B. | 若m>n,则碱性 X(OH)m>Y(OH)n | |
| C. | 若半径aXm+>bYn+,则a<b | |
| D. | 若半径aXm+>bY n+,则X的单质一定能从含Yn+的盐溶液中置换出Y |
分析 离子aXm+、bY n+、cZP-、dWk-都具有相同的电子层结构,则应存在a-m=b-n=c+p=d+k,且X、Y为金属,Z、W为非金属性,X、Y在Z、W的下一周期,
A.若P>K,则原子序数W>Z,同周期随原子序数增大非金属性增强,非金属性越强,阴离子的还原性越弱;
B.若m>n,则原子序数X>Y,同周期随原子序数增大金属性减弱,金属性越强,最高价氧化物对应水化物的碱性越强;
C.电子层结构相同,核电荷数越大离子半径越小;
D.若X为Na,X的单质不能能从含Yn+的盐溶液中置换出Y.
解答 解:离子aXm+、bY n+、cZP-、dWk-都具有相同的电子层结构,则应存在a-m=b-n=c+p=d+k,且X、Y为金属,Z、W为非金属性,X、Y在Z、W的下一周期,
A.若P>K,则c<d,非金属性Z<W,元素的非金属性越强,对应的阴离子的还原性越弱,故A错误;
B.若m>n,金属性X<Y,碱性X(OH)m<Y(OH)n,故B错误;
C.核电荷数越大离子半径越小,半径aXm+>bY n+,则a<b,故C正确;
D.核电荷数越大离子半径越小,若半径aXm+>bY n+,则X核电荷数较小,金属性较强,如X能与水反应,则不能置换出Y,故D错误.
故选C.
点评 本题考查结构与位置关系、元素周期律等,难度中等,根据电荷与核外电子排布相同推断元素在周期表中的位置是关键.

练习册系列答案
相关题目
19.用电火花点燃装在一密闭容器中的一种气态烃和足量的氧气,完全燃烧后,容器内气体体积保持不变(气体体积均在120℃和相同的压强下测定),这种气态烃不可能是( )
| A. | CH4 | B. | C2H4 | C. | C3H4 | D. | C3H6 |
17.下列说法中正确的是( )
| A. | Na2O2分子中所有原子最外层均达到8电子稳定结构 | |
| B. | NH4Cl、MgCl2均为离子化合物,均含有离子键和共价键 | |
| C. | 同周期第ⅠA族元素和第ⅦA族元素之间只能形成离子化合物 | |
| D. | NH4Cl仅由非金属元素组成,所以它是共价化合物 |
4.研究表明生命起源于火山爆发,是因为火山爆发产生的气体中含有1%的羰基硫(COS),已知羰基硫分子中所有原子均满足八电子结构,结合周期表知识,有关说法不正确的是( )
| A. | 羰基硫分子为非极性分子 | |
| B. | 羰基硫的结构式为:O=C=S | |
| C. | 羰基硫沸点比CO2高 | |
| D. | 羰基硫分子中三个原子处于同一直线上 |
14.化合物丙由如下反应得到: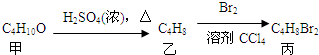 ,丙的结构简式不可能是( )
,丙的结构简式不可能是( )
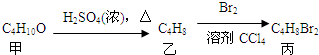 ,丙的结构简式不可能是( )
,丙的结构简式不可能是( )| A. | CH3CH2CHBrCH2Br | B. | CH3CH(CH2Br)2 | C. | CH3CHBrCHBrCH3 | D. | (CH3)2CBrCH2Br |
1.对于${\;}_{19}^{40}$K原子,下列叙述不正确的是( )
| A. | 原子核内质子数为19 | B. | 原子核外电子数为19 | ||
| C. | 质量数为40 | D. | 中子数为40 |
18.用下列一种试剂就可鉴别出甲酸、乙酸、甲酸乙酯和乙酸甲酯,该试剂是( )
| A. | 银氨溶液 | B. | 新制Cu(OH)2悬浊液 | C. | KMnO4(H+)溶液 | D. | NaOH溶液 |
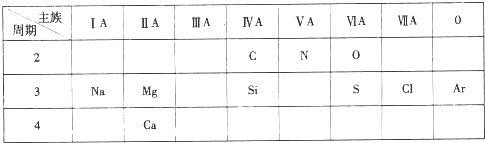
 ;
;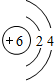 ,元素C在周期表中的位置为第三周期ⅣA族,E的元素名称为氯.
,元素C在周期表中的位置为第三周期ⅣA族,E的元素名称为氯.