题目内容
已知1—18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,则下列叙述或表示方法正确的是( )
| A.四种元素位于同一周期 | B.氢化物的稳定性:H2Y>HZ |
| C.离子的氧化性:aW3+>bX+ | D.a+3=c-2 |
C
解析试题分析:aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,即这四种微粒的核外电子数相等。A.由于阳离子是原子失去电子形成的,形成的离子比原子少一个电子层;阴离子是原子获得电子形成的,离子的电子层数与原子相同。所以四种元素位于不同的周期。错误。B.由于Z、Y在同一周期,非金属性Z>Y。元素的非金属性越强,其对应的氢化物就越温度。故氢化物的稳定性: HZ >H2Y。错误。C.对于电子层结构相同的离子来说,离子的核电荷数越大,离子的半径就越小,离子的氧化性就越强。由于核电荷数离子aW3+>bX+,所以离子的的氧化性:aW3+>bX+。正确。D. aW3+是原子失去3个电子形成的,cY2-是原子获得2个电子形成的,由于二者的电子数相等,所以a-3=c+2.错误。
考点:考查电子层结构相同的微粒的有关性质的知识。

 名校课堂系列答案
名校课堂系列答案下列元素中,不属于主族元素的是( )
| A.钡 | B.铁 | C.钙 | D.碘 |
氡是放射性稀有气体元素,氡气吸入体内有害健康,氡的核电荷数是86,相对原子质量是222。科学家还发现某些放射性矿物分解放出的“锕射气”,是由质子数86,质量数219的原子组成,下列有关氡的说法正确的是
A.氡气在标准状况下密度约是19.82g |
| B.氡气化学性质较活泼,因此对人体有害 |
| C.氡原子核外有7个电子层,最外层有8个电子 |
| D.“锕射气”是氡的同位素 |
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中不正确的是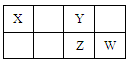
| A.Y与Z形成的化合物是形成酸雨的原因之一 |
| B.W的单质能与水反应,生成一种具有漂白性的物质 |
| C.最高价氧化物对应水化物的酸性:W >Z >X |
| D.气态氢化物的稳定性:W > Z >Y |
.运用元素周期律分析下面的推断,其中错误的是
| A.砹(85号元素)是一种有色固体,HAt应该不稳定,且AgAt是有色难溶于水固体 |
| B.铍(Be)是一种金属,它的氧化物的水化物可能具有两性 |
| C.硫酸锶(SrSO4)是难溶于水和盐酸的的白色固体 |
| D.硒化氢(H2Se)是无色、有毒、比H2S稳定的气体 |
X、Y、Z、W为四种短周期主族元素,它们在周期表中的相对位置如图所示。Z元素原子核外K层与M层电子数相等。下列说法中正确的是
| | | X | Y |
| Z | W | | |
A.Y元素最高价氧化物对应的水化物化学式为H2YO3
B.原子半径由小到大的顺序为:Y<X<W<Z
C.室温下,Z和W的单质均能溶于浓硝酸
D.X、Z两种元素的氧化物中所含化学键类型相同
短周期元素X、Y、Z三种原子核外电子总数为32,都可形成常温下气体单质。X原子最外层电子数是其内层电子数的3倍;Y的气态氢化物与其最高价氧化物对应的水化物恰好反应的产物只有一种A,A的水溶液显酸性。下列说法正确的是
| A.原子半径: Z>X >Y |
| B.X元素形成的单质其摩尔质量一定是32g·moL-1 |
| C.物质A中既含离子键又含共价键 |
| D.YX2、ZX2都有对应的含氧酸 |
X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价代数和为6。下列说法正确的是
| A.Y元素最高价氧化物对应的水化物化学式H2YO4 |
| B.原子半径由大到小的顺序为:Z>Y> W |
| C.X、Z两种元素的气态氢化物中,Z的气态氢化物较稳定 |
| D.X与W形成的两种化合物中,阴、阳离子物质的量之比均为1︰2 |