题目内容
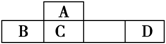
X、Y、Z、W为四种短周期主族元素,它们在周期表中的相对位置如图所示。Z元素原子核外K层与M层电子数相等。下列说法中正确的是
| | | X | Y |
| Z | W | | |
A.Y元素最高价氧化物对应的水化物化学式为H2YO3
B.原子半径由小到大的顺序为:Y<X<W<Z
C.室温下,Z和W的单质均能溶于浓硝酸
D.X、Z两种元素的氧化物中所含化学键类型相同
B
解析试题分析:X、Y、Z、W为C、N、Mg、Al。A、N对应的最高价氧化物对应的水化物化学式为HNO3,错误;B、电子层数多半径大,同周期从左到右原子半径减小,正确;C、常温下铝在浓硫酸、浓硝酸中钝化,错误;D、对应的氧化物为二氧化碳和氧化镁,分别为共价化合物和离子化合物,错误。
考点:考查原子结构与元素周期律有关问题。

练习册系列答案
相关题目
已知1—18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,则下列叙述或表示方法正确的是( )
| A.四种元素位于同一周期 | B.氢化物的稳定性:H2Y>HZ |
| C.离子的氧化性:aW3+>bX+ | D.a+3=c-2 |
已知下列元素的原子半径如下表所示: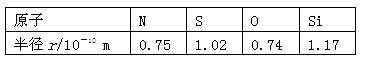
根据以上数据,磷原子的半径可能是
| A.1.10 ×10-10 m | B.0.80×10-10 m | C.1.20× 0-10 m | D.0.70×10-10 m |
下列有关物质性质的比较顺序中,不正确的是 ( )
| A.微粒半径:K+>Na+>Mg2+>Al3+ |
| B.热稳定性:HF<HCl<HBr<HI |
| C.酸性:HClO4>H2SO4>H3PO4>H2SiO3 |
| D.熔点:Li>Na>K>Rb |
X、Y、Z、M、W为五种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的1/2。下列说法正确的是
| A.原子半径:W>Z>Y>X>M |
| B.XZ2、X2M2、W2Z2均为直线型的共价化合物 |
| C.由X元素形成的单质不一定是原子晶体 |
| D.由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |