��Ŀ����
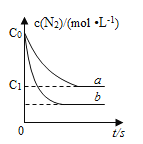
����Ŀ�������£���һԪ�� HA ����Һ�� KOH ��Һ��������(��������仯)��ʵ���������±���
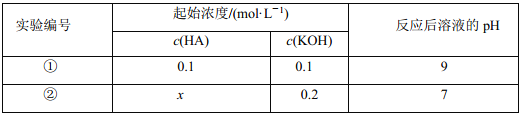
�����жϲ���ȷ����( )
A��ʵ������Ӧ�����Һ�У�c(K+)>c(A��)>c(OH��)>c(H+)
B��ʵ������Ӧ�����Һ�У�c(OH��)��c(K+)��c(A��)��![]()
C��ʵ������Ӧ�����Һ�У�c(A��)+c(HA)>0.1 mol/L
D��ʵ������Ӧ�����Һ�У�c(K+)��c(A��)>c(OH��)��c(H+)
���𰸡� B
��������
��������������£����������Ũ�ȵ�HA��KOH���(��������仯)����Һ�ʼ��ԣ�˵�����������ᡣA����Һ�д��ڵ���غ㣬��c(K+)+c(H+)=c(A-)+c(OH-)��������ǿ�������Σ�����Һ�ʼ��ԣ�c(OH-)��c(H+)��ˮ�ĵ������������c(A-)��c(OH-)����A��ȷ��B����Һ�д��ڵ���غ㣬��c(K+)+c(H+)=c(A-)+c(OH-)��c(OH-)-c(H+)=c(K+)-c(A-)=![]() mol/L-10-9 mol/L����B����C���������ʵ�������ͼ�ǡ�÷�Ӧʱ����Һ�ʼ��ԣ�Ҫʹ���������ͼ��Ϻ���Һ�����ԣ������Ũ��Ӧ���ڼ���������غ��c(A-)+c(HA)��0.1 mol/L����C��ȷ��D����Һ�д��ڵ���غ㣬��c(K+)+c(H+)=c(A-)+c(OH-)����Һ�����ԣ���c(OH-)=c(H+)����c(K+)=c(A-)��������Һ��ˮ�ĵ������������c(A-)��c(OH-)����D��ȷ����ѡB��
mol/L-10-9 mol/L����B����C���������ʵ�������ͼ�ǡ�÷�Ӧʱ����Һ�ʼ��ԣ�Ҫʹ���������ͼ��Ϻ���Һ�����ԣ������Ũ��Ӧ���ڼ���������غ��c(A-)+c(HA)��0.1 mol/L����C��ȷ��D����Һ�д��ڵ���غ㣬��c(K+)+c(H+)=c(A-)+c(OH-)����Һ�����ԣ���c(OH-)=c(H+)����c(K+)=c(A-)��������Һ��ˮ�ĵ������������c(A-)��c(OH-)����D��ȷ����ѡB��

����Ŀ����ѧ��Ӧ���������������������������
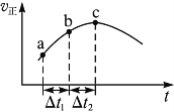
��1��Aѧ��Ϊ��̽��п�����ᷴӦ�����е����ʱ仯������200mLϡ�����м���������п�ۣ�����ˮ�������ռ���Ӧ�ų���������ʵ���¼���£��ۼ�ֵ����
ʱ�䣨min�� | 1 | 2 | 3 | 4 | 5 |
���������mL������״���� | 100 | 240 | 464 | 576 | 620 |
�ٷ�Ӧ��������ʱ����ǣ�ָ0��1��1��2��2��3��3��4��4��5 ��____min��ԭ����_________________��
����2��3����ʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����________________��������Һ������䣩
��2��Bѧ��Ҳ��ͬ����ʵ�飬�����ڷ�Ӧ̫�죬�ⲻ�������������취���ͷ�Ӧ���ʣ��������ѡ���������м�������__________�Լ�����Ӧ���ʡ�����д���ţ�
A������ˮ B������ C��HNO3��Һ D��CuSO4��Һ
��3��ij�¶�����10L�ܱ������У�3����̬����A��B��C�����ʵ�����ʱ��仯������ͼ��

�ٸ÷�Ӧ�Ļ�ѧ����ʽ��________��
�����ڸ������ﵽ��Ӧ���ȣ�ƽ��״̬��ʱ��Ӧ���ת���ʡ�ת����=��ת�������ʵ���/��ʼ���ʵ�������100%������д��������̣�����������1λС����________