题目内容
碳、硅同为周期表中ⅣA族的元素,是构成自然界各种物质的重要元素.
(一)由碳元素构成的各种单质和化合物都是科学家研究的重要对象.
(1)用特殊方法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下方法提纯,请配平该反应的化学方程式:
______C+______KMnO4+______H2SO4→______CO2↑+______MnSO4+______K2SO4+______H2O
(2)汽车尾气中的一氧化碳是大气污染物,可通过反应:CO(g)+
O2(g)?CO2(g)降低其浓度.
①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如下表所示.请填写表中的空格.
②相同温度下,某汽车尾气中CO、CO2的浓度分别为1.0×10-5mol/L和1.0×10-4mol/L.若在汽车的排气管上增加一个补燃器,不断补充O2并使其浓度保持为1.0×10-4mol/L,则最终尾气中CO的浓度为______mol/L(请保留两位有效数字).
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9.CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mol/L,则生成沉淀所需CaCl2溶液的最小浓度为______.
(二)晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用过量的碳还原二氧化硅制得粗硅
②粗硅与干燥的HCl气体反应制得SiHCl3
③SiHCl3与过量的H2在1000℃~1100℃反应制得纯硅,已知SiHCl3能与水强烈反应,在空气中易自燃.请回答:
(1)第一步制取粗硅的化学方程式______.
(2)粗硅与HCl反应制备三氯氢硅的过程中发生反应的热化学方程式为:
(i)Si(s)+3HCl(g)═SiHCl3(g)+H2(g)△H=-210kJ/mol
(ii)Si(s)+4HCl(g)═SiCl4(g)+2H2(g)(副反应)△H=-241kJ/mol
①常温下,SiHCl3和SiCl4均为液态化合物,二者互溶且均易水解,则分离二者的最佳方法是______.
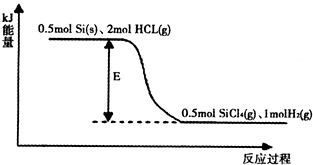
②某反应的能量变化如图所示:则该反应的能量变化E=______kJ.
③SiCl4可转化为SiHCl3而循环使用,则该反应的热化学方程式为:______.
(一)由碳元素构成的各种单质和化合物都是科学家研究的重要对象.
(1)用特殊方法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下方法提纯,请配平该反应的化学方程式:
______C+______KMnO4+______H2SO4→______CO2↑+______MnSO4+______K2SO4+______H2O
(2)汽车尾气中的一氧化碳是大气污染物,可通过反应:CO(g)+
| 1 |
| 2 |
①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如下表所示.请填写表中的空格.
| 容器编号 | c(CO)/mol?L-1 | c(O2)mol?L-1 | c(CO2)mol?L-1 | v(正)和v(逆)比较 |
| Ⅰ | 2.0×10-4 | 4.0×10-4 | 4.0×10-2 | v(正)=v(逆) |
| Ⅱ | 3.0×10-4 | 4.0×10-4 | 5.0×10-2 | v(正)______v(逆) |
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9.CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4mol/L,则生成沉淀所需CaCl2溶液的最小浓度为______.
(二)晶体硅是一种重要的非金属材料,制备纯硅的主要步骤如下:
①高温下用过量的碳还原二氧化硅制得粗硅
②粗硅与干燥的HCl气体反应制得SiHCl3
③SiHCl3与过量的H2在1000℃~1100℃反应制得纯硅,已知SiHCl3能与水强烈反应,在空气中易自燃.请回答:
(1)第一步制取粗硅的化学方程式______.
(2)粗硅与HCl反应制备三氯氢硅的过程中发生反应的热化学方程式为:
(i)Si(s)+3HCl(g)═SiHCl3(g)+H2(g)△H=-210kJ/mol
(ii)Si(s)+4HCl(g)═SiCl4(g)+2H2(g)(副反应)△H=-241kJ/mol
①常温下,SiHCl3和SiCl4均为液态化合物,二者互溶且均易水解,则分离二者的最佳方法是______.
②某反应的能量变化如图所示:则该反应的能量变化E=______kJ.

③SiCl4可转化为SiHCl3而循环使用,则该反应的热化学方程式为:______.
(一)(1)高锰酸钾中锰元素化合价降低7-2=5价,碳元素化合价升高4-0=4价,化合价升高数=化合价降低数,所以高锰酸钾前的系数是4,碳单质前的系数是5,根据原子守恒,二氧化碳前是5,硫酸锰前是4,硫酸钾前面是2,根据硫酸跟守恒,所以硫酸前面是6,据氧原子和氢原子守恒,产物少6个水分子,
故答案为:5;4;6;5;4;2;6;
(2)①由Ⅰ可求K=
=104L
?mol
,
由Ⅱ可求Q=
=
×104L
?mol
<K,
故平衡右移,v(正)>v(逆),
故答案为:>;
②CO(g)+
O2(g)?CO2(g).
起始 1.0×10-5mol 01.0×10-4mol
△n nmol
nmol nmol
平衡1.0×10-5mol-nmol 1.0×10-4mol 1.0×10-4mol+nmol
则K=
=104,
解得,n=8.91×10-6mol/L,
故CO浓度为1.0×10-5mol-8.91×10-6mol=1.1×10-6mol/L,
故答案为:1.1×10-6.
(3)Na2CO3溶液的浓度为2×10-4mol/L,等体积混合后溶液中c(CO32-)=
×2×10-4mol/L=1×10-4mol/L,根据Ksp=c(CO32-)?c(Ca2+)=2.8×10-9可知,
c(Ca2+)=
mol/L=2.8×10-5mol/L,
原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,
故原溶液CaCl2溶液的最小浓度为2×2.8×10-5mol/L=5.6×10-5mol/L.
故答案为:5.6×10-5mol/L.
(二)(1)高温下用碳还原二氧化硅生成硅与一氧化碳,反应方程式为SiO2+2C
Si+2CO↑,
故答案为:SiO2+2C
Si+2CO↑;
(2)①HCl易溶于水,而SiHCl3与H2O强烈反应,故提纯SiHCl3的方法只能在无水的条件下利用它们的沸点不同,采用分馏的方法进行,
故答案为:蒸馏;
②反应热化学方程式为:Si(s)+4HCl(g)═SiCl4(g)+2H2(g)(副反应)△H=-241kJ/mol,若反应0.5mol硅和2molHCl,则放出120.5kJ热量,
故答案为:120.5;
③将(i)-(ii)可得SiCl4(g)+H2(g)═SiHCl3(g)+HCl(g)△H1=+31kJ/mol,
故答案为:SiCl4(g)+H2(g)═SiHCl3(g)+HCl(g)△H1=+31kJ/mol;
故答案为:5;4;6;5;4;2;6;
(2)①由Ⅰ可求K=
| 4.0×10-2mol/L | ||
2.0×10-4mol/L×
|
| 1 |
| 2 |
| 1 |
| 2 |
由Ⅱ可求Q=
| 5.0×10-2mol/L | ||
3.0×10-4mol/L×
|
| 5 |
| 6 |
| 1 |
| 2 |
| 1 |
| 2 |
故平衡右移,v(正)>v(逆),
故答案为:>;
②CO(g)+
| 1 |
| 2 |
起始 1.0×10-5mol 01.0×10-4mol
△n nmol
| 1 |
| 2 |
平衡1.0×10-5mol-nmol 1.0×10-4mol 1.0×10-4mol+nmol
则K=
| 1.0×10-4+n |
| 1.0×10-4×(1.0×10-5-n) |
解得,n=8.91×10-6mol/L,
故CO浓度为1.0×10-5mol-8.91×10-6mol=1.1×10-6mol/L,
故答案为:1.1×10-6.
(3)Na2CO3溶液的浓度为2×10-4mol/L,等体积混合后溶液中c(CO32-)=
| 1 |
| 2 |
c(Ca2+)=
| 2.8×10-9 |
| 1×10-4 |
原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,
故原溶液CaCl2溶液的最小浓度为2×2.8×10-5mol/L=5.6×10-5mol/L.
故答案为:5.6×10-5mol/L.
(二)(1)高温下用碳还原二氧化硅生成硅与一氧化碳,反应方程式为SiO2+2C
| ||
故答案为:SiO2+2C
| ||
(2)①HCl易溶于水,而SiHCl3与H2O强烈反应,故提纯SiHCl3的方法只能在无水的条件下利用它们的沸点不同,采用分馏的方法进行,
故答案为:蒸馏;
②反应热化学方程式为:Si(s)+4HCl(g)═SiCl4(g)+2H2(g)(副反应)△H=-241kJ/mol,若反应0.5mol硅和2molHCl,则放出120.5kJ热量,
故答案为:120.5;
③将(i)-(ii)可得SiCl4(g)+H2(g)═SiHCl3(g)+HCl(g)△H1=+31kJ/mol,
故答案为:SiCl4(g)+H2(g)═SiHCl3(g)+HCl(g)△H1=+31kJ/mol;

练习册系列答案
相关题目