题目内容
【题目】下列关于物质的用途及反应方程式的叙述不正确的是( )
A.印刷电路板时用FeCl3作为腐蚀液:2Fe3+ + Cu == 2Fe2+ + Cu2+
B.用HF雕刻玻璃:SiO2 + 4HF == SiF4↑ + 2H2O
C.高炉炼铁的主要原理:CO + FeO == Fe + CO2
D.小苏打做发酵粉:2NaHCO3 == Na2CO3 + H2O + CO2↑
【答案】C
【解析】
A. 制作印刷电路板时用FeCl3作为腐蚀液,氯化铁和铜反应生成氯化亚铁和氯化铜,反应的离子方程式是2Fe3+ + Cu == 2Fe2+ + Cu2+,故A正确;
B. 二氧化硅与氢氟酸反应生成四氟化硅气体和水,用HF雕刻玻璃的化学方程式是SiO2 + 4HF == SiF4↑ + 2H2O,故B正确;
C. 高炉炼铁的主要原理是高温条件下用一氧化碳还原氧化铁,反应方程式是3CO + Fe2O3 ![]() 2Fe + 3CO2,故C错误;
2Fe + 3CO2,故C错误;
D. 碳酸氢钠加热分解为碳酸钠、二氧化碳、水,小苏打做发酵粉的反应方程式是2NaHCO3 ![]() Na2CO3 + H2O + CO2↑,故D正确;
Na2CO3 + H2O + CO2↑,故D正确;
故答案选C。

【题目】下述实验方案能达到实验结果的是( )
编号 | A | B | C | D |
实验方案 |
|
片刻后在 |
|
置于光亮处 |
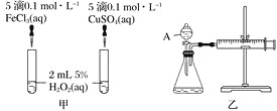
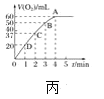
实验结果 | 铁钉发生析氢反应 |
| 左球气体颜色加深; 右球气体颜色变浅 | 甲烷与氯气发生加成反应 |
A.AB.BC.CD.D
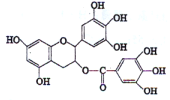
【题目】肉桂酸是生产冠心病药物“心可安”的重要中间体。其酯类衍生物是配制香精和食品香料的重要原料。它在农用塑料和感光树脂等精细化工产品的生产中也有着广泛的应用。实验室合成肉桂酸的反应原理如下

部分物质的相关性质如下表所示:
名称 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 主要性质 |
苯甲醛 | 106.0 | -26 | 179 | 纯品为无色液体,微溶于水;空气中加热易被缓慢氧化 |
乙酸酐 | 102.0 | -73.1 | 138.6 | 无色透明液体;有剌激性气味;其蒸气为催泪毒气,遇水强烈水解生成乙酸,产生大量酸雾 |
肉桂酸 | 148.0 | 133 | 300 | 白色至淡黄色粉末;微有桂皮香气 |
石蜡 | / | 50-70 | 300-550 | 主要由烷烃组成,性质稳定 |
实验步骤如下:
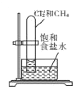
步骤1:适量无水醋酸钾、14.5mL乙酸酐(过量)和5.0mL苯甲醛(密度为1.06g/cm3)依次加入150ml三颈烧瓶中摇匀,放入磁子,搭好回流装置,用带磁力搅拌功能的电炉(图A)加热至微沸后保持加热回流1小时;
步骤2:取下三口烧瓶,冷却至100度以下后,加入少量饱和碳酸钠溶液调节pH8-9;
步骤3:如图B连接好水蒸气蒸馏装置(加热装置略去),进行水蒸气蒸馏,直至馏出物无油滴;
步骤4:将三口烧瓶中的残余液冷却后加入活性炭,煮沸,____往滤液中边搅拌边滴加浓盐酸至pH=3,大量固体析出;
步骤5:减压过滤,洗涤,烘干,称量,测熔点。
回答下列问题:
(1)步骤1中,若用酒精灯加热,可能存在的安全隐患是__。
(2)步骤2中,加饱和碳酸钠溶液的目的是___,可观察到的明显现象是__。
(3)步骤3中,水蒸气蒸馏的目的是除去__。(填物质名称)
(4)步骤4中,缺失的操作名称是__。
(5)步骤5中,若称量得到的产品质量为4.800g,则本实验的产率为__%(保留4位有效数字)。

(6)有机都有固定的熔点,因此测量产品的熔点可以初步判定所得的产品是不是预期产物。测产品熔点的装置如图C所示:将产品装入一端封口的毛细玻璃管中,与温度计绑在一起,插入b形管(图D)中,用火焰持续加热b形管右侧,观察毛细管中样品的状态以及相应温度计的示数,即可测得样品的熔程(刚开始出现液滴至恰好完全熔化的温度范围)。测定过程中,温度计的水银球应位于__(填“m”、“n”或“p”),b形管中所装的热浴液可选用__(填相应字母编号)。
A.蒸馏水 B.浓硫酸 C.石蜡