题目内容
胡妥油(D)用作香料的原料,它可由A合成得到:
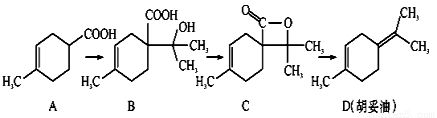
A.从B到C的反应是消去反应
B.D分子中所有碳原子一定共面
C.等物质的量的B分别与足量的Na、NaHCO3反应,产生的气体的物质的量前者大于后者
D.若A是由2-甲基-1,3-丁二烯和内烯酸(CH2=CHCOOH)加热得到的,则该反应的类型属于加成反应
练习册系列答案
相关题目
17.如表有关实验现象、解释和结论都正确的一项是( )
| 实验操作 | 实验现象 | 解释或结论 | |
| A | 加热(170℃)乙醇与浓硫酸混合物,将产生的气体直接通入酸性高锰酸钾溶液 | 酸性高锰酸钾溶液紫红色逐渐变浅 | 可能产生了SO2气体 |
| B | 取少量KI溶液,先滴加氯水,再加入少量苯,振荡、静置 | 溶液分为两层,下层是紫红色 | KI和氯水及苯发生反应 |
| C | 将少量SO2通入苯酚钠溶液中,振荡 | 溶液中出现浑浊 | 因为发生了反应: C6H5O-+SO2+H2O═C6H5OH+HSO3- |
| D | 把浓氨水加入到盛有Cu2O的试管中 | 溶液先无色,静置一段时间后变成蓝色 | Cu+被空气氧化成了Cu2+、使溶液显蓝色 |
| A. | A | B. | B | C. | C | D. | D |
18.有关化学用语正确的是( )
| A. | Be原子的结构示意图: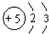 | |
| B. | 二氧化硅的分子式:SiO2 | |
| C. | 质子数为53、中子数为78的碘原子可表示为:53131I | |
| D. | 乙烯的结构式:CH2=CH2 |
15.25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1 mol•L-1CH3COOH与0.1 mol•L-1氨水等体积混合(pH=7): c(NH4+)=c(CH3COO-)=c(H+)=c(OH-) | |
| B. | 0.1 mol•L-1HCl溶液与0.2 mol•L-1氨水等体积混合(pH>7): c(NH4+)>c(Cl-)>c(NH3•H2O)>c(OH-) | |
| C. | 0.1 mol•L-1CH3COONa溶液与0.1 mol•L-1CaCl2溶液等体积混合: c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) | |
| D. | 0.1 mol•L-1Na2CO3溶液与0.1 mol•L-1 NaHCO3溶液等体积混合: c(HCO3-)>0.05 mol•L-1>c(CO32-)>c(OH-) |
20.固体乙醇晶体中不存在的作用力是( )
| A. | 氢键 | B. | 极性键 | C. | 非极性键 | D. | 离子键 |
9.将足量的CO2通入下列溶液中,最终溶液浑浊的是( )
①饱和苏打溶液 ②水玻璃 ③氯化钡 ④次氯酸钙.
①饱和苏打溶液 ②水玻璃 ③氯化钡 ④次氯酸钙.
| A. | ①② | B. | ③④ | C. | ②③ | D. | ①②③④ |
16.下列有关实验装置进行的相应实验,能达到实验目的是( )

| A. | 用图1所示装置制取干燥的氨气 | |
| B. | 图2装置可用于制取少量纯净的CO2气体 | |
| C. | 用图3所示装置将溶液定容到100 mL | |
| D. | 图4装置可用于比较碳酸钠和碳酸氢钠的热稳定性,大试管A中装碳酸钠固体,小试管B中装碳酸氢钠固体 |
13.下列有关物质性质的描述和该性质的应用均正确的是( )
| A. | 铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 | |
| B. | 氢氟酸具有强酸性,用氢氟酸蚀刻玻璃 | |
| C. | 过氧化钠只有氧化性,用过氧化钠为潜水艇舱提供氧气 | |
| D. | FeCl3具有氧化性,用FeCl3溶液刻蚀印刷电路板 |
14.下列实验现象和原因都正确且有因果关系的是( )
| 选项 | 实验操作及现象 | 产生现象的原因 |
| A | 在氯化银浊液中滴加几滴稀KI溶液,白色沉淀变黄色 | 氯化银的溶度积小于碘化银的溶度积 |
| B | 在新制的氯水中滴加紫色石蕊溶液,溶液先变红色后褪色 | 氯水中有次氯酸,先电离出H+,使石蕊变红;后氧化有色物质 |
| C | 氨气通入酚酞溶液中,溶液变红色 | 氨气是一种碱,在水中电离出OH- |
| D | 借助导线,铜片和锌片在稀硫酸中构成原电池的两个电极,铜极表面产生气泡,锌极溶解 | 锌比铜活泼,锌失去电子,电子经外电路流向铜片,氢离子从铜片获得电子,最终产生氢气 |
| A. | A | B. | B | C. | C | D. | D |

