题目内容
【题目】下列说法中正确的是( )
A. 氨分子是三角锥形,而甲烷是正四面体形,是因为NH3分子中有一对未成键的孤电子对,它对成键电子的排斥作用较强
B. 杂化轨道全部参加形成化学键
C. PCl5分子中P原子和Cl原子最外层都满足8电子结构
D. 在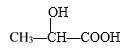 分子中含有2个手性C原子
分子中含有2个手性C原子
【答案】A
【解析】
A项、氨分子中氮原子的价层电子对数为4,孤对电子数为1,杂化轨道为sp3杂化,孤对电子对成键电子的排斥作用较强,N-H之间的键角小于109°28′,所以氨气分子空间构型是三角锥形;甲烷分子中碳原子的价层电子对数为4,孤对电子数为0,杂化轨道为sp3杂化,碳原子连接4个相同的原子,C-H之间的键角相等为109°28′,故CH4为正四面体构型,故A正确;
B项、杂化轨道可以部分参加形成化学键,例如氨分子中氮原子杂化轨道为sp3杂化,形成了4个sp3杂化轨道,但是只有3个参与形成化学键,故B错误;
C项、在化合物中,原子最外层电子数等于原子的价层电子数+|化合价|,PCl5中P原子的最外层电子为:5+5=10,Cl原子的最外层电子为:7+|-1|=8,不都满足8电子稳定结构,故C错误;
D项、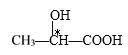 分子中,带*号碳原子所连的四个取代基分别是羟基、甲基、氢原子和羧基,该碳原子具有手性,分子中含有1个手性C原子,故D错误。
分子中,带*号碳原子所连的四个取代基分别是羟基、甲基、氢原子和羧基,该碳原子具有手性,分子中含有1个手性C原子,故D错误。
答案选A。

练习册系列答案
相关题目