题目内容
【题目】(1)在①CO2,②NaCl,③Na,④Si,⑤CS2,⑥金刚石,⑦(NH4)2SO4,⑧乙醇中,由极性键形成的非极性分子有_______(填序号,以下同),含有金属离子的物质是__,分子间可形成氢键的物质是________,属于离子晶体的是__,属于原子晶体的是__,①~⑤五种物质的熔点由高到低的顺序是__。
(2)A,B,C,D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2,不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3500 ℃
试推断它们的晶体类型:A.__;B.__;C.__;D.__。
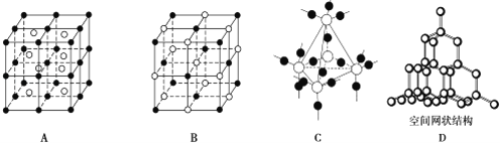
(3)下图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:A.__;B.__;C.__D.____。
.
【答案】①⑤ ②③ ⑧ ②⑦ ④⑥ ④>②>③>⑤>① 金属晶体 分子晶体 离子晶体 原子晶体 氯化铯 氯化钠 二氧化硅 金刚石(或晶体硅)
【解析】
(1)根据组成元素及微粒之间的化学键分析;根据晶体的熔点:原子晶体>离子晶体>金属晶体>分子晶体;
(2)根据晶体的物理性质分析晶体类型;
(3)根据晶体结构模型判断物质的种类。
(1) ①CO2⑤CS2中只含有极性键,分子都是直线形分子,正负电荷中心重合,属于非极性分子;由极性键形成的非极性分子有①⑤;
②NaCl是由钠离子和氯离子构成;③Na是由钠离子和自由电子构成,都含有金属离子;含有金属离子的物质是②③;
⑧乙醇中羟基氢与羟基上的氧原子能形成氢键;分子间可形成氢键的物质是⑧;
②NaCl由钠离子和氯离子构成,属于离子化合物;⑦(NH4)2SO4由铵根离子和硫酸根离子构成,属于离子化合物;离子化合物在固态时均为离子晶体;属于离子晶体的是②⑦;
④Si⑥金刚石都是由原子构成的原子晶体;属于原子晶体的是④⑥;
晶体的熔点:原子晶体>离子晶体>金属晶体>分子晶体,Si和金刚石都是原子晶体,原子半径越小,共价键越强,熔点越高,CO2和CS2都是分子晶体,相对分子质量越大熔点越高,Na的熔点低于100℃,,所以熔点高到低的顺序为: ④>②>③>⑤>①;
综上所述,本题答案是: ①⑤; ②③; ⑧; ②⑦; ④⑥; ④>②>③>⑤>①。
(2)A.固态时能导电,能溶于盐酸,属于活泼金属,属于金属晶体;
B.能溶于CS2,不溶于水,属于分子晶体;
C.固态时不导电,液态时能导电,可溶于水,属于离子晶体;
D.固态、液态时均不导电,熔点为3500 ℃,属于原子晶体;
综上所述,本题答案是:金属晶体,分子晶体,离子晶体,原子晶体。
(3)由晶胞结构模型可知:在氯化铯晶体中,每个Cs+同时吸引8个Cl-,每个Cl-吸引8个Cs+,而氯离子与铯离子数目之比为1:1,故A为氯化铯;
在氯化钠晶体中,每个Na+同时吸引着6个Cl-,每个Cl-吸引着6个Na+,而氯离子与钠离子的数目之比为1:1,故B为氯化钠晶体;
在二氧化硅晶体中,每个Si原子与4个O原子结合,每个O原子与2个Si原子,硅原子与氧原子的个数比为1:2,故C为SiO2;
在金刚石晶体中,每个碳原子周围紧邻4个碳原子,最小碳环由6个碳原子组成,故D为金刚石;(晶体硅的结构和金刚石相似)。
由晶胞结构模型可以知道A、B、C、D分别为氯化铯、氯化钠、二氧化硅、金刚石(或晶体硅);
综上所述,本题答案是:氯化铯,氯化钠,二氧化硅,金刚石(或晶体硅)。