题目内容
【题目】磷酸亚铁锂(LiFePO4)可用作锂离子电池正极材料,具有热稳定性好、循环性能优良、安全性高等特点,文献报道可采用FeCl3、NH4H2PO4、LiCl和苯胺等作为原料制备。回答下列问题:
(1)在周期表中,与Li的化学性质最相似的邻族元素是________,该元素基态原子核外M层电子的自旋状态_________(填“相同”或“相反”)。
(2)FeCl3中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的FeCl3的结构式为____,其中Fe的配位数为_____________。
(3) NH4H2PO4中P的_______杂化轨道与O的2p轨道形成 σ 键。
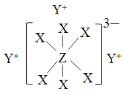
(4)NH4H2PO4和LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示:
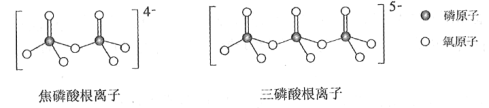
这类磷酸根离子的化学式可用通式表示为____________(用n代表P原子数)。
【答案】Mg 相反 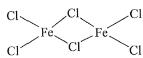 4 sp3 (PnO3n+1)(n+2)—
4 sp3 (PnO3n+1)(n+2)—
【解析】
(1)根据对角线原则分析可得;
(2)在氯化铁双聚分子中,铁原子除了与3个氯原子形成共价键外,还能接受另一氯原子提供的孤对电子而形成配位键;
(3)NH4H2PO4是由铵根离子和磷酸二氢根离子形成的离子化合物,磷酸二氢根离子中P原子的价层电子对数为4;
(4)可以根据磷酸根、焦磷酸根、三磷酸根的化学式寻求规律分析。
(1)根据对角线原则可知与锂的化学性质相似的是镁,镁元素基态原子核外M层的电子数是2,价电子排布式为43s2,s轨道的2个电子自旋方向相反,故答案为:Mg;相反;
(2)在氯化铁双聚分子中,铁原子除了与3个氯原子形成共价键外,还能接受另一氯原子提供的孤对电子而形成配位键,则双聚分子存在的FeCl3的结构式为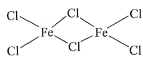 ,每个铁原子与4个氯原子相连,则Fe的配位数为4,故答案为:
,每个铁原子与4个氯原子相连,则Fe的配位数为4,故答案为: ;4;
;4;
(3)NH4H2PO4是由铵根离子和磷酸二氢根离子形成的离子化合物,磷酸二氢根离子中P原子的价层电子对数为4,采取sp3杂化,sp3杂化轨道与O的2p轨道形成 σ 键,故答案为:sp3;
(4)磷酸根、焦磷酸根、三磷酸根的化学式分别为PO42-、P2O74 -、P3O105-,由化学式可知磷原子的变化规律为1、2、3。。。n,氧原子的变化规律为4、7、。。。3n+1,酸根的电荷数变化规律为3、4、5。。。n+2,则这类磷酸根离子化学式的通式为(PNO3N+1)(n+2)-,故答案为:(PnO3n+1)(n+2)-。

 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案