题目内容
18.HClO是比H2CO3还弱的酸,当反应Cl2+H2O?HCl+HClO达到平衡后,要使HClO的浓度增加,可加入( )| A. | NaOH固体 | B. | NaCl固体 | C. | H2O | D. | CaCO3固体 |
分析 当反应Cl2+H2O?HCl+HClO达到平衡后,要使HClO的浓度增加,可以加入能和稀盐酸反应的物质促进平衡向右移动,据此分析解答.
解答 解:A.NaOH是强碱,和HCl、HClO都反应,加入NaOH固体后虽然平衡正向移动,但HClO浓度降低,故A错误;
B.氯化钠中含有氯离子,加入氯化钠后,溶液中氯离子浓度增大,抑制平衡移动,所以HClO浓度降低,故B错误;
C.加水稀释促进平衡正向移动,但参加反应的氯气增大程度小于溶液体积增大程度,所以HClO浓度降低,故C错误;
D.因为HClO是比H2CO3还弱的酸,所以碳酸钙和稀盐酸反应但和次氯酸不反应,加入碳酸钙后,盐酸参加反应参加平衡正向移动,次氯酸不反应导致其浓度增大,故D正确;
故选D.
点评 本题考查弱电解质的电离,侧重考查学生分析判断及获取信息利用信息能力,“HClO是比H2CO3还弱的酸”隐含着碳酸盐和次氯酸不反应,易错选项是C.

练习册系列答案
相关题目
8.生活中的一些问题常涉及到化学知识,下列叙述正确的是( )
| A. | 苯、汽油、无水乙醇都是纯净物 | |
| B. | 甘油易溶于水,可用于制炸药TNT | |
| C. | 福尔马林和苯酚都是良好的杀菌剂,都可用于饮用水及环境消毒 | |
| D. | 室内装饰材料中缓慢释放出的甲醛、苯等有机物会污染空气 |
9.下列物质不能发生水解反应的是( )
| A. | 乙酸乙酯 | B. | 淀粉 | C. | 蛋白质 | D. | 乙酸 |
6.利用下列装置(部分仪器已省略),能顺利完成对应实验的是( )
| A. | 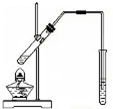 制硝基苯 | B. |  制氢氧化亚铁 | C. | 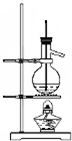 实验室制乙烯 | D. | 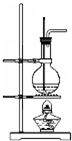 石油的蒸馏 |
13.下列离子方程式正确的是( )
| A. | 实验室用大理石与醋酸反应制取二氧化碳:CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 氯乙酸与足量的氢氧化钠溶液共热:CH2ClCOOH+OH-→CH2ClCOO-+H2O | |
| C. | 苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO${\;}_{3}^{2-}$ | |
| D. | 用银氨溶液检验乙醛中的醛基:CH3CHO+2[Ag(NH3)2]++2OH- $\stackrel{水浴加热}{→}$CH3COO--+NH4++3NH3+2Ag↓+H2O |
3.已知汽车尾气无害化处理反应为:2NO(g)+2CO (g)?N2(g)+2CO2(g).下列说法错误的是( )
| A. | 通入大量 NO,ν 正、ν 逆 均增大 | |
| B. | 恒温恒容下充入 Ne,ν 正、ν 逆 均不变 | |
| C. | ν 正(NO)=2ν 逆(N2)时,反应达到平衡 | |
| D. | n (NO):n (CO):n (N2):n (CO2)=2:2:1:2 时,反应达到平衡 |
10.下列烯烃中存在顺反异构体的是( )
| A. | 2-甲基-2-丁烯 | B. | 2-戊烯 | C. | 1-丁烯 | D. | 丙烯 |
7.下列事实,可以证明氨水是弱碱的是( )
| A. | 氨水能跟氯化亚铁溶液反应生成氢氧化亚铁 | |
| B. | 铵盐受热易分解 | |
| C. | 0.1mol/L的氨水可以使酚酞试液变红 | |
| D. | 0.1mol/L的NH4Cl溶液的pH约为5 |
8.25℃时,将0.02 mol•L-1的HCOOH溶液与0.01mol•L-1的NaOH溶液等体积混合,所得溶液的pH<7.则下列关系式中不正确的是( )
| A. | c(HCOO-)>c(Na+) | B. | c(HCOOH)<c(HCOO-) | ||
| C. | c(HCOOH)+c(HCOO-)=0.02mol•L-1 | D. | 2c(H+)+c(HCOOH)=c(HCOO-)+2c(OH-) |