题目内容
书写下列离子方程式
(1)氢氧化钡和硫酸在溶液中反应
(2)氯气通入水中反应
(3)向碳酸氢钠溶液中加入过量的澄清石灰水 .
(1)氢氧化钡和硫酸在溶液中反应
(2)氯气通入水中反应
(3)向碳酸氢钠溶液中加入过量的澄清石灰水
考点:离子方程式的书写
专题:离子反应专题
分析:(1)氢氧化钡与硫酸反应生成硫酸钡沉淀和水;
(2)氯气与水反应生成氯化氢和次氯酸,次氯酸需要保留分子式;
(3)碳酸氢钠和过量石灰水反应,碳酸氢钠全部反应生成碳酸钙沉淀.
(2)氯气与水反应生成氯化氢和次氯酸,次氯酸需要保留分子式;
(3)碳酸氢钠和过量石灰水反应,碳酸氢钠全部反应生成碳酸钙沉淀.
解答:
解:(1)氢氧化钡和硫酸在溶液中反应生成硫酸钡和水,反应的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,
故答案为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O;
(2)氯气通入水中反应生成氯化氢和次氯酸,反应的离子方程式为:Cl2+H2O=Cl-+H++HClO,
故答案为:Cl2+H2O=Cl-+H++HClO;
(3)碳酸氢钠溶液中加入过量的澄清石灰水,碳酸氢钠全部反应,反应的离子方程式为:HCO3-+Ca2++OH-═CaCO3↓+H2O,
故答案为:HCO3-+Ca2++OH-═CaCO3↓+H2O.
故答案为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O;
(2)氯气通入水中反应生成氯化氢和次氯酸,反应的离子方程式为:Cl2+H2O=Cl-+H++HClO,
故答案为:Cl2+H2O=Cl-+H++HClO;
(3)碳酸氢钠溶液中加入过量的澄清石灰水,碳酸氢钠全部反应,反应的离子方程式为:HCO3-+Ca2++OH-═CaCO3↓+H2O,
故答案为:HCO3-+Ca2++OH-═CaCO3↓+H2O.
点评:本题考查了离子方程式的书写,该题是高考中的高频题,为中等难度的试题,注意掌握离子方程式的书写原则,如难溶物、弱电解质、氧化物等需要保留化学式,必须满足守恒关系(如:质量守恒和电荷守恒等).

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
X、Y、Z、W、R5种主族元素属3个短周期,且原子半径依次减小.X、R同主族不相邻,可行形成离子化合物XR;Y、Z同主族,Y元素原子的最外层电子数是其电子层数的2倍,关于上述各元素及其化合物的下列叙述不正确的是( )
| A、非金属性:Y<Z<W |
| B、Z、R按原子数1:1形成的化合物不稳定,易分解 |
| C、X分别与Y、Z、W、R形成的二元化合物,溶于水所得溶液有的呈中性,有的呈碱性 |
| D、元素Z、W按原子数1:2形成的化合物中各原子均为最外层8电子稳定结构 |
下列分子中,所有原子都满足最外层为8电子结构的是( )
| A、H2O |
| B、XeF4 |
| C、CCl4 |
| D、SO2 |
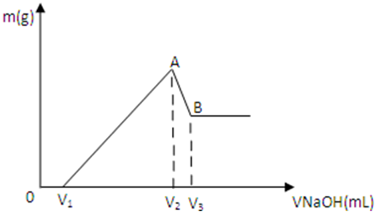 将0.1mol Mg、Al混合物溶于100mL 3mol/L HCl中,再滴加1mol/L NaOH溶液,在滴加NaOH溶液的过程中,沉淀的质量m随NaOH溶液体积V变化如图所示:
将0.1mol Mg、Al混合物溶于100mL 3mol/L HCl中,再滴加1mol/L NaOH溶液,在滴加NaOH溶液的过程中,沉淀的质量m随NaOH溶液体积V变化如图所示: 某种胃药片的制酸剂为碳酸钙,其中所含的制酸剂质量的测定如下:
某种胃药片的制酸剂为碳酸钙,其中所含的制酸剂质量的测定如下: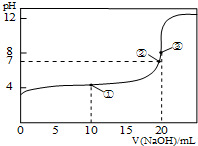 已知醋酸是日常生活中常见的弱酸.
已知醋酸是日常生活中常见的弱酸.