题目内容
在加热的条件下,用MnO2与足量的浓盐酸反应,制得标况下的氯气11.2L.(MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O).
求:(1)需要消耗MnO2多少克?
(2)被氧化的HCl的物质的量是多少?
| ||
求:(1)需要消耗MnO2多少克?
(2)被氧化的HCl的物质的量是多少?
考点:化学方程式的有关计算
专题:计算题
分析:(1)根据氯气的体积计算其物质的量,代入化学反应方程式来计算二氧化锰的物质的量,再利用m=n×M来计算;
(2)被氧化的HCl生成氯气,根据氯原子守恒计算被氧化HCl的物质的量.
(2)被氧化的HCl生成氯气,根据氯原子守恒计算被氧化HCl的物质的量.
解答:
解:(1)标况下,11.2L氯气的物质的量=
=0.5mol,
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
1 1
0.5mol 0.5mol
则m(MnO2)=0.5mol×87g.mol-1=43.5g,
答:需要消耗43.5g MnO2.
(2)被氧化的HCl生成氯气,则被氧化的HCl的物质的量=2n(Cl2)=2×0.5mol=1mol,
答:被氧化的HCl的物质的量是1mol.
| 11.2L |
| 22.4L/mol |
MnO2+4HCl(浓)
| ||
1 1
0.5mol 0.5mol
则m(MnO2)=0.5mol×87g.mol-1=43.5g,
答:需要消耗43.5g MnO2.
(2)被氧化的HCl生成氯气,则被氧化的HCl的物质的量=2n(Cl2)=2×0.5mol=1mol,
答:被氧化的HCl的物质的量是1mol.
点评:本题考查化学反应方程式的有关计算、氧化还原反应计算,比较基础,注意从化合价的变化判断被氧化的HCl的物质的量.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
100mL 6mol?L-1的H2SO4溶液跟过量锌粉反应,在一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
①Na2CO3溶液 ②水 ③K2SO4溶液 ④KNO3溶液.
①Na2CO3溶液 ②水 ③K2SO4溶液 ④KNO3溶液.
| A、①③ | B、②③ | C、①④ | D、②④ |
下列各操作中,正确的是( )
| A、为减缓反应速率,用饱和食盐水与电石反应制乙炔 |
| B、制备乙烯:实验室用无水乙醇和浓硫酸共热到170℃制取乙烯 |
| C、浓硫酸的稀释:应将蒸馏水加入到浓硫酸中 |
| D、用酒精萃取碘水中的碘 |
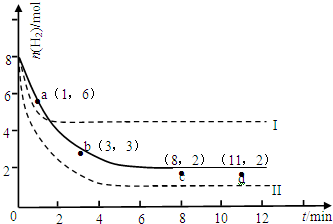 工业上也可以用CO2和H2反应制得甲醇.在2×105Pa、300℃的条件下,若有44g CO2与6g H2恰好完全反应生成气体甲醇和水,放出49.5kJ的热量.试写出该反应的热化学方程式:
工业上也可以用CO2和H2反应制得甲醇.在2×105Pa、300℃的条件下,若有44g CO2与6g H2恰好完全反应生成气体甲醇和水,放出49.5kJ的热量.试写出该反应的热化学方程式: