题目内容
下列分子中,所有原子都满足最外层为8电子结构的是( )
| A、H2O |
| B、XeF4 |
| C、CCl4 |
| D、SO2 |
考点:原子核外电子排布
专题:原子组成与结构专题
分析:对于共价化合物,原子最外层电子数=元素化合价绝对值+元素原子的最外层电子层=8,则该元素原子满足8电子结构,含H元素的化合物一定不满足,据此判断.
解答:
解:A.H2O中H原子不满足8电子结构,故A错误;
B.XeF4中Xe原子最外层电子数=4+8=12,不满足8电子结构,故B错误;
C.CCl4中C原子最外层电子数=4+4=8,Cl原子最外层电子数=|-1|+7=8,都满足8电子结构,故C正确;
D.SO2中S原子最外层电子数=4+6=10,不满足8电子结构,故D错误,
故选C.
B.XeF4中Xe原子最外层电子数=4+8=12,不满足8电子结构,故B错误;
C.CCl4中C原子最外层电子数=4+4=8,Cl原子最外层电子数=|-1|+7=8,都满足8电子结构,故C正确;
D.SO2中S原子最外层电子数=4+6=10,不满足8电子结构,故D错误,
故选C.
点评:本题考查对共价键理解、8电子结构判断,注意利用化合价与最外层电子数来分析解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列有关胶体的说法不正确的是( )
| A、向Fe(OH)3胶体中滴加过量的稀硫酸,会产生红褐色沉淀 |
| B、葡萄糖注射液不能产生丁达尔现象,不属于胶体 |
| C、向污水中投放明矾,生成能凝聚悬浮物的胶体:Al3++3H2O?Al(OH)3(胶体)+3H+ |
| D、在水泥和冶金工厂常用高压电除去大量烟尘,以减少对空气的污染化学在生产和日 |
在短周期中,R原子最外层电子数是其次外层电子数的3倍,下列说法不正确的是( )
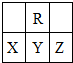

| A、原子半径大小:X>Y>Z |
| B、氢化物的稳定性:X>Y |
| C、化合物YR2能使品红溶液褪色 |
| D、X、Y、Z三种元素最高价氧化物的水化物的酸性最强的是Z |
下列反应的离子方程式正确的是( )
| A、AlCl3溶液中滴加足量氨水:Al3++4OH-═AlO2-+2H2O |
| B、氢氧化钙悬浊液中滴加盐酸:H++OH-═H2O |
| C、NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
| D、MaSO4溶液中加入Ba(OH)2溶液:SO42-+Ba2+═BaSO4↓ |
下列符号所代表的微粒不影响水的电离平衡的是( )
A、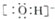 |
| B、HCO3- |
C、 |
D、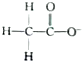 |