题目内容
6.化学兴趣小组的同学为测定某Na2CO3和NaCl的固体混合物样品中Na2CO3的质量分数进行了以下实验,请你参与并完成对有关问题的解答.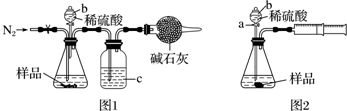
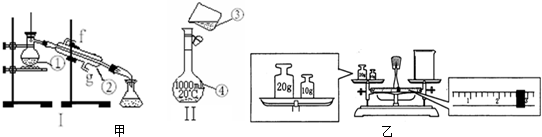
(1)甲同学用图1所示装置测定CO2的质量.实验时稀硫酸是与样品中的Na2CO3(填“Na2CO3”或“NaCl”)发生反应,仪器b的名称是分液漏斗,洗气瓶c中盛装的是浓硫酸,此浓硫酸的作用是除去CO2中的水蒸气.
(2)乙同学用图2所示装置,取一定质量的样品(m g)和足量稀硫酸反应进行实验,完成样品中Na2CO3质量分数的测定.
①实验前,检查该装置气密性的方法是先打开活塞a,由b注入水至其下端玻璃管中形成一段水柱,再将针筒活塞向内推压,若b下端玻璃管中的液面上升,则装置气密性良好.
②在实验完成时,能直接测得的数据是CO2的体积(填“体积”或“质量”).
(3)丙同学用如图所示方法和步骤进行实验:
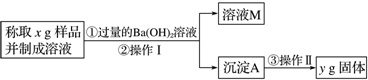
①操作Ⅰ涉及的实验名称有过滤、洗涤;操作Ⅱ涉及的实验名称有干燥、称量.
②丙同学测得的样品中Na2CO3质量分数的计算式为$\frac{106y}{197x}$×100%.
分析 (1)依据装置和试剂分析,硫酸和样品中的碳酸钠反应,仪器b是加入液体的仪器可以控制加入的量,是分液漏斗;反应过程中含有水蒸气,可以利用浓硫酸干燥二氧化碳气体;
(2)①使用注射器改变瓶内气体的多少而改变瓶内压强;当将针筒活塞向内推压时,瓶内气体被压缩,压强增大,瓶内液体则会被压入长颈漏斗内,b下端玻璃管中液面上升,可以说明装置气密性良好;
②装置中 加入硫酸和碳酸钠反应生成二氧化碳,注射器活塞被向外推出,可以测定二氧化碳的体积;
(3)①依据流程分析可知,加入氢氧化钡溶液和碳酸钠 反应生成碳酸钡沉淀,通过过滤得到沉淀,洗涤后称重得到沉淀碳酸钡质量;
②依据沉淀质量计算物质的量,依据碳元素守恒计算碳酸钠质量,计算样品中碳酸钠的质量分数.
解答 解:(1)依据装置和试剂分析,硫酸和样品中的碳酸钠反应,仪器b是加入液体的仪器可以控制加入的量,是分液漏斗;反应过程中含有水蒸气,可以利用浓硫酸干燥二氧化碳气体,
故答案为:Na2CO3;分液漏斗;除去CO2中的水蒸气;
(2)①使用注射器改变瓶内气体的多少而改变瓶内压强;当将针筒活塞向内推压时,瓶内气体被压缩,压强增大,瓶内液体则会被压入长颈漏斗内,b下端玻璃管中液面上升,可以说明装置气密性良好,
故答案为:液面上升;
②在实验完成时,反应后可以利用注射器读取生成气体的体积,能直接测得的数据是CO2的体积,
故答案为:体积;
(3)①流程分析可知,加入氢氧化钡溶液和碳酸钠 反应生成碳酸钡沉淀,通过过滤得到沉淀,洗涤后称重得到沉淀碳酸钡质量,
故答案为:过滤;称量;
②流程分析判断沉淀质量为yg,物质的量=$\frac{yg}{197g/mol}$=$\frac{y}{197}$mol;碳酸钠物质的量和碳酸钡物质的量相同,样品质量为Xg,则碳酸钠质量为$\frac{y}{197}$mol×106g/mol;
所以碳酸钠的质量分数=$\frac{\frac{106y}{197}}{x}$×100%=$\frac{106y}{197x}$×100%,
故答案为:$\frac{106y}{197x}$×100%.
点评 本题考查了物质性质的实验验证和含量测定方法分析判断,混合物中物质质量分数的计算方法和应用,题目难度中等,答题时注意元素化合物知识和实验基本操作的灵活运用.

| A. | Na原子结构示意图: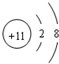 | B. | 乙烷的结构简式:CH3CH3 | ||
| C. | HClO的结构式:H-Cl-O | D. | CH4分子的比例模型: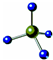 |
| A. | 过氧化钙(CaO2)的电子式: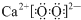 | |
| B. | ${\;}_8^{16}{O^{2-}}$离子的结构示意图: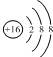 | |
| C. | 质子数为94、中子数为144的钚(Pu)原子:${\;}_{94}^{144}$Pu | |
| D. | 葡萄糖的结构简式:C6H12O6 |
| A. | 将Cu投入稀硫酸中 | |
| B. | 让Cu在潮湿的环境发生电化学腐蚀 | |
| C. | 将Cu投入浓硫酸中并加热 | |
| D. | 用Cu作电极、稀硫酸作电解质溶液电解 |
①CH3CH2Cl、②
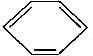 ③(CH3)2C═CH2④
③(CH3)2C═CH2④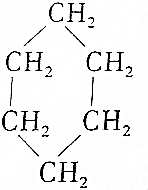 ⑤
⑤
| A. | 链状烃:①③⑤ | B. | 链状烃:①③ | C. | 环状烃:②④⑤ | D. | 芳香烃:②④ |
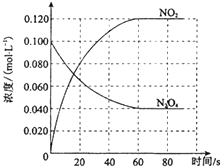 在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)═2NO2(g)△H,随温度升高,混合气体的颜色变深.
在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)═2NO2(g)△H,随温度升高,混合气体的颜色变深.