题目内容
15.将铁和氧化铁的混合物3.84g投入足量稀H2SO4溶液中,充分反应后收集到672 mL H2,向溶液中滴入KSCN,无现象.气体体积在标准状况下测定,求原混合物中铁和氧化铁的质量.分析 Fe、Fe2O3 的混合物与硫酸恰好完全反应,生成了铁的硫酸盐,反应后反应加入KSCN 溶液,无血红色出现,说明只生成FeSO4,发生反应为:Fe+H2SO4=FeSO4+H2↑、Fe+Fe2O3+3H2SO4=3FeSO4+3H2O,根据生成的氢气计算与硫酸反应的Fe的质量,进而计算与硫酸反应的Fe、Fe2O3 的总质量,二者物质的量之比为1:1,计算各自物质的量,再计算混合物中Fe、氧化铁的质量.
解答 解:Fe、Fe2O3 的混合物与硫酸恰好完全反应,生成了铁的硫酸盐,反应后反应加入KSCN 溶液,无血红色出现,说明只生成FeSO4,发生反应为:Fe+H2SO4=FeSO4+H2↑、Fe+Fe2O3+3H2SO4=3FeSO4+3H2O,
n(H2)=$\frac{0.672L}{22.4L/mol}$=0.03mol,则:
Fe+H2SO4=FeSO4+H2↑
1 1
n(Fe) 0.03mol
n(Fe)=0.03mol,m(Fe)=0.03mol×56g/mol=1.68g,
故硫酸反应的Fe、Fe2O3 的质量为3.84g-1.68=2.16g,
由反应Fe+Fe2O3+3H2SO4=3FeSO4+3H2O可知知二者物质的量之比为1:1,故n′(Fe)=n(Fe2O3)=$\frac{2.16g}{56g/mol+160g/mol}$=0.01mol,
则混合物中含有铁的物质的量为:0.03mol+0.01mol=0.04mol,质量为:56g/mol×0.04mol=2.24g;
混合物中含有氧化铁的质量为:160g/mol×0.01mol=1.6g,
答:原混合物中铁和氧化铁的质量分别为2.24g、1.6g.
点评 本题考查混合物计算、根据方程式计算,题目难度中等,明确发生反应的原理为解答关键,注意Fe在反应中发生与硫酸反应、与硫酸铁反应,试题培养了学生的分析能力及化学计算能力.

| A. | 0.15mol/L的H2SO4溶液 | B. | 0.2mol/L醋酸 | ||
| C. | 0.2mol/L的HCl溶液 | D. | 0.2mol/L的NaOH溶液 |
| A. | Na2CO3比NaHCO3稳定得多 | |
| B. | NaHCO3比Na2CO3难溶于水 | |
| C. | 用物质的量相同的苏打和小苏打可得到相同质量的CO2 | |
| D. | 石灰水既能和Na2CO3反应,又能与NaHCO3反应,且反应原理相同 |
| A. | 氢氧化铁与盐酸反应OH-+H+═H2O | |
| B. | 次氯酸钠溶液中通入少量CO2 2ClO-+CO2+H2O═2HClO+CO${\;}_{3}^{2-}$ | |
| C. | 硫酸氢钠溶液中加入氢氧化钡溶液至沉淀完全 Ba2++OH-+H++SO${\;}_{4}^{2-}$═BaSO4↓+H2O | |
| D. | 钠与水反应 Na+2H2O═Na++2OH-+H2↑ |
| 元素代号 | I1 | I2 | I3 | I4 |
| A | 2080 | 4000 | 6100 | 9400 |
| B | 500 | 4600 | 6900 | 9500 |
| C | 740 | 1500 | 7700 | 10500 |
| D | 580 | 1800 | 2700 | 11600 |
(2)B通常显+1价,B的电负性<C的电负性(填“>”、“<”或“=”).(3)元素C的第一电离能比D高的原因是镁的外围电子为3S2,处于全充满状态,能量较低,较稳定,所需第一电离能较大
(4)下列元素中,化学性质和物理性质最像A元素的是A.
A.氦(1s2) B.铍(1s22s2) C.锂(1s221) D.氢(1s1) (5)每种元素都出现相邻两个电离能的数据相差较大的情况,请你估计B的第2次电离 能飞跃数据将是第9电子.
①晨雾中看见叶缝透过光束的通路 ②用明矾净水 ③一支钢笔使用不同牌号的蓝黑墨水易出现堵塞 ④静电除尘 ⑤豆浆做豆花 ⑥血液透析 ⑦在江河入海口处容易形成沙洲( )
| A. | ①②⑤⑦ | B. | ①③④⑤⑥ | C. | ①③⑤⑥⑦ | D. | 全部都有关 |
| A. | 1.0L1.0mo1•L-1的NaNO3水溶液中含有的氧原子数为3NA | |
| B. | 0.1molCu与足量的浓硫酸反应生成SO2的体积为2.24L | |
| C. | 25℃时pH=13的Ba(OH)2溶液中含有OH一的数目为0.1NA | |
| D. | 反应Cl2+2NaOH=NaCl+NaClO+H2O中,每消耗1molCl2转移电子数为 NA |
(1)①相同条件下,2mol SO2和1mol O2所具有的能量>(填“>”、“<”或“=”)2mol SO3具有的能量;
②在相同条件下,若断开2mol SO2、1molO2和2mol SO3中的化学键时,吸收的能量分别为Q1、Q2、Q3,则Q1+Q2<Q3(填“>”、“<”或“=”);
③在一定条件下,当该反应生成2molSO3时,放出197kJ的热量,该条件下,如果将3mol SO2和1mol O2混合,使其充分反应,放出的热量<197kJ(填“>”、“<”或“=”),反应达到平衡后,n(SO2)+n(SO3)=3mol.
(2)科研人员设想用如图所示装置生产硫酸,
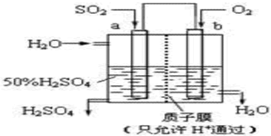
①通入O2的b极是原电池正极(填“正”或“负”);
②电解质溶液中阴离子向a极移动(填“a”或“b”);
③负极反应式为2SO2-4e-+4H2O=2SO42-+8H+.
(3)将一定量的SO2和含0.7mol氧气的空气(忽略CO2)放入0.5L密闭容器内,550℃时,在催化剂作用下充分发生反应.测得n(O2)随时间的变化如下表
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(O2)/mol | 0.7 | 0.4 | 0.3 | x | x | x |
请回答下列问题:
①用O2表示从1~2s内该反应的平均反应速率为0.2mol•L-1•s-1;
②该反应达到平衡时,SO2的转化率为90%(用百分数表示);
③该反应达到平衡时,O2的体积分数是6.2%(用百分数表示);
④若反应在绝热密闭系统中进行时,其余条件不变,反应速率是先增大后减小,其原因可能是:该反应是放热反应,反应开始后放出的热量使体系的温度升高,反应速率加快;一段时间后,随着浓度的减小,化学反应速率减慢.