题目内容
【题目】下表是四种盐在不同温度下的溶解度(g/100g水):(假设:盐类共存时不影响各自的溶解度,分离晶体时,溶剂的损耗忽略不计)
NaNO3 | KNO3 | NaCl | KCl | |
10℃ | 80.5 | 21.2 | 35.7 | 31.0 |
100℃ | 175 | 246 | 39.1 | 56.6 |
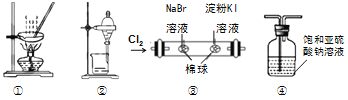
用物质的量之比为1:1的硝酸钠和氯化钾为原料,制取硝酸钾晶体,其流程如图所示

以下说法错误的是( )
A.①和②的实验过程中,都需要控制温度
B.①实验操作依次为:加水溶解、蒸发浓缩结晶、趁热过滤
C.②实验操作依次为:加水溶解、蒸发浓缩结晶、趁热过滤
D.用95%的酒精洗涤所得的硝酸钾晶体比较好
【答案】C
【解析】
由分离流程可知,因硝酸钠和氯化钾不同温度下溶解度不同,在①的实验过程中,将硝酸钠和氯化钾加水溶解,蒸发浓缩,有NaCl析出,趁热过滤分离出氯化钠,将滤液冷却可使硝酸钾析出,以此来解答。
A. ①为蒸发浓缩,②为冷却结晶,均需要控制温度,故A正确;
B. ①实验分离出NaCl,操作依次为:加水溶解、蒸发浓缩结晶、趁热过滤,故B正确;
C. ②实验操作为冷却结晶,故C错误;
D. 用95%的酒精洗涤所得的硝酸钾晶体比较好,可减少硝酸钾的溶解,故D正确;
答案选C。

练习册系列答案
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案
相关题目