题目内容
20.X、Y、Z、W是中学化学中常见的四种气体.已知:X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收;X是化石燃料燃烧的产物之一,是形成酸雨的物质;Y是一种单质,它的水溶液具有漂白作用;Z是硝酸工业和汽车尾气中的有害物质之一,呈现红棕色,并能与水反应;W气体的水溶液滴入酚酞变红色.请回答下列问题:
(1)写出各物质的化学式XSO2,YCl2,ZNO2,WNH3;
(2)X、Y两种气体按物质的量之比1:1的比例通入品红溶液中,品红不褪色,原因Cl2+SO2+2H2O=2HCl+H2SO4(用化学方程式表示);
(3)在Z与水的反应中,氧化剂与还原剂的物质的量之比为1:2.
(4)W和Z在催化剂的作用下可以转化成两种无污染的物质,反应方程式:6NO2+8NH3$\frac{\underline{\;催化剂\;}}{\;}$7N2+12H2O.
分析 X、Y、Z、W是中学化学中常见的四种气体.X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收,X是化石燃料燃烧的产物之一,是形成酸雨的物质,则X为SO2;Y是一种单质,它的水溶液具有漂白作用,则Y为Cl2;Z是硝酸工业和汽车尾气中的有害物质之一,呈现红棕色,则Z为NO2,W气体的水溶液滴入酚酞变红色,溶液呈碱性,则W为NH3,据此解答.
解答 解:(1)X、Y、Z、W是中学化学中常见的四种气体.X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收,X是化石燃料燃烧的产物之一,是形成酸雨的物质,则X为SO2;Y是一种单质,它的水溶液具有漂白作用,则Y为Cl2;Z是硝酸工业和汽车尾气中的有害物质之一,呈现红棕色,则Z为NO2,W气体的水溶液滴入酚酞变红色,溶液呈碱性,则W为NH3,
故答案为:SO2;Cl2;NO2;NH3;
(2)SO2、Cl2两种气体按物质的量之比1:1的比例通入品红溶液中,发生反应:Cl2+SO2+2H2O=2HCl+H2SO4,氯气与二氧化硫恰好反应,品红不褪色,
故答案为:不褪色;Cl2+SO2+2H2O=2HCl+H2SO4;
(3)NO2与水发生反应:3NO2+H2O=2HNO3+NO,氧化剂与还原剂均为二氧化氮,氧化剂生成NO、还原剂得到硝酸,可知氧化剂与还原剂的物质的量之比为1:2,
故答案为:1:2;
(4)NO2、NH3在催化剂的作用下可以转化成两种无污染的物质,反应生成氮气与水,反应方程式为:6NO2+8NH3$\frac{\underline{\;催化剂\;}}{\;}$7N2+12H2O,
故答案为:6NO2+8NH3$\frac{\underline{\;催化剂\;}}{\;}$7N2+12H2O.
点评 本题考查无机物推断,充分根据物质的性质推断,需要学生熟练掌握元素化合物性质,难度不大.

| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳、氢原子个数比为1:2 | ||
| C. | 无法确定该化合物是否含有氧元素 | D. | 该化合物中一定含有氧元素 |
| A. | 结构式 | B. | 电子式 | C. | 球棍模型 | D. | 比例模型 |
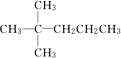 ,并对其命名2,2-二甲基戊烷.其中另一种同分异构体分子是由烯烃和氢气加成得到,而且该烯烃分子中的碳碳双键只有一种位置,试写出这种烯烃分子的名称3,3-二甲基-1-戊烯.
,并对其命名2,2-二甲基戊烷.其中另一种同分异构体分子是由烯烃和氢气加成得到,而且该烯烃分子中的碳碳双键只有一种位置,试写出这种烯烃分子的名称3,3-二甲基-1-戊烯. 2C(g)ΔH<0,下列图象正确的是
2C(g)ΔH<0,下列图象正确的是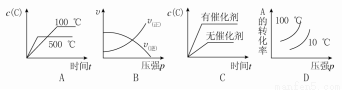
 可以被KMnO4的酸性溶液氧化生成
可以被KMnO4的酸性溶液氧化生成  ,但若烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到
,但若烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到  .
.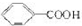 的异构体共有7种,其中的3种是
的异构体共有7种,其中的3种是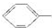 CH2CH2CH2CH2,
CH2CH2CH2CH2,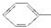 CH(CH2)CH2CH2CH2,
CH(CH2)CH2CH2CH2, CH2CH(CH2)CH2CH2
CH2CH(CH2)CH2CH2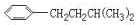 、
、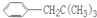 、
、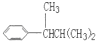 、
、 .
.