题目内容
17.元素周期表中前7周期的元素数目如下表所示:| 周期数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 元素数 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
(2)周期表中第ⅢB族所含元素最多,第ⅣA族元素形成化合物种类最多.
(3)请分析周期数与元素数的关系,预言第8周期最多可能含有元素种数为C.
A.18 B.32 C.50 D.64.
分析 (1)第六、七周期在第ⅢB族中出现了镧系、锕系,每个系的一个空格包含了15种元素;
(2)第六、七周期在第ⅢB族中出现了镧系、锕系,故ⅢB族含有元素最低;碳元素形成有机物,化合物种类最多;
(3)观察每一周期的元素数发现,它们都是偶数,规律如下:
| 周 期 数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 元 素 数 | 2 2×1 2×12 | 8 2×4 2×22 | 8 2×4 2×22 | 18 2×9 2×32 | 18 2×9 2×32 | 32 2×16 2×42 | 32 2×16 2×42 |
解答 解:(1)第六、七周期在第ⅢB族中出现了镧系、锕系,每个系的一个空格包含了15种元素,第六、七周期比第四、五周期多了14种元素,
故答案为:第六、七周期在第ⅢB族中出现了镧系、锕系;
(2)第六、七周期在第ⅢB族中出现了镧系、锕系,每个系的一个空格包含了15种元素,故ⅢB族含有元素最低;碳元素形成有机物,化合物种类最多,处于第ⅣA,
故答案为:第ⅢB;第ⅣA;
(3)观察每一周期的元素数发现,它们都是偶数,规律如下:
| 周 期 数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 元 素 数 | 2 2×1 2×12 | 8 2×4 2×22 | 8 2×4 2×22 | 18 2×9 2×32 | 18 2×9 2×32 | 32 2×16 2×42 | 32 2×16 2×42 |
故选:C.
点评 本题考查元素周期表与元素周期律,难度中等,侧重考查学生分析推理能力及同主族元素化合物性质的相似性与递变性,注意对对数学归纳法的应用.

练习册系列答案
相关题目
7.香花石由前20号元素中的6种组成,其化学式为X3Y2(ZWR4)3T2,X、Y、Z为金属元素,Z的最外层电子数与次外层相等,X、Z位于同主族,Y、Z、R、T位于同周期,R最外层电子数为次外层的3倍,T无正价,X与R原子序数之和是W的2倍.下列说法不正确的是( )
| A. | 原子半径:Y>Z>R>T | |
| B. | 气态氢化物的稳定性:W<R<T | |
| C. | 最高价氧化物对应的水化物碱性:X>Y>Z | |
| D. | XR2、WR2两化合物中R的化合价相同 |
8.下列反应中,铁只能生成高价化合物的是( )
| A. | 少量铁与稀硫酸反应 | B. | 铁丝在氧气中燃烧 | ||
| C. | 过量铁粉在氯气中燃烧 | D. | Fe投入到CuSO4溶液中 |
5.下列溶液中通入SO2后,最终一定会出现沉淀的是( )
| A. | HCl和Ba(NO3)2的混合溶液 | B. | BaCl2溶液 | ||
| C. | NaOH溶液 | D. | Ca(OH)2溶液 |
2.现有物质的量浓度均为 0.1mol•L -1 的下列五种物质的溶液:①HCl ②H2SO4③CH3COOH ④NH4Cl ⑤NaOH.其溶液中由水电离出的c(H+)的大小关系是( )
| A. | ①=②>③>④>⑤ | B. | ④>③>①=⑤>② | C. | ③>①>②>④>⑤ | D. | ④>③>①>⑤>② |
6.已知草酸(H2C2O4)是一种二元弱酸,主要用作还原剂和漂白剂.
(1)草酸的电离方程式为H2C2O4?H++HC2O4-,HC2O4-?H++C2O42-.
(2)将草酸溶液与酸性高锰酸钾溶液混合发生的反应为:
MnO4-+H2C2O4+6H+→Mn2++CO2↑+H2O
某合作小组同学在烧杯中进行上述反应时,发现刚开始一段时间,反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快.
①配平上述离子方程式
②该实验不久后溶液突然褪色的原因最有可能是C.
A.体系压强增大 B.反应物接触面积增大
C.生成物对反应有催化作用 D.反应物浓度增大
(3)为研究该化学反应速率的影响因素,某同学进行了以下实验:
①对比实验1和3要研究改变反应物浓度对化学反应速率的影响,请完成表格中横线.
②实验2中溶液褪色时间t 为D
A.>40 B.=40 C.<40 D.无法判断.
(1)草酸的电离方程式为H2C2O4?H++HC2O4-,HC2O4-?H++C2O42-.
(2)将草酸溶液与酸性高锰酸钾溶液混合发生的反应为:
MnO4-+H2C2O4+6H+→Mn2++CO2↑+H2O
某合作小组同学在烧杯中进行上述反应时,发现刚开始一段时间,反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快.
①配平上述离子方程式
②该实验不久后溶液突然褪色的原因最有可能是C.
A.体系压强增大 B.反应物接触面积增大
C.生成物对反应有催化作用 D.反应物浓度增大
(3)为研究该化学反应速率的影响因素,某同学进行了以下实验:
| 组别 | 温度/℃ | V(H2C2O4) /mL | V(KMnO4) /mL | V(H2O) /mL | KMnO4溶液 褪色时间/s |
| 1 | 30 | 10 | 10 | 20 | 40 |
| 2 | 30 | 20 | 20 | 0 | t |
| 3 | 30 | 15 | 10 | 15 |
②实验2中溶液褪色时间t 为D
A.>40 B.=40 C.<40 D.无法判断.
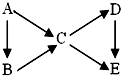 A为单质,B、C、D、E为与A含有相同元素的化合物,它们之间有如下转化关系:
A为单质,B、C、D、E为与A含有相同元素的化合物,它们之间有如下转化关系:
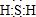 ;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O弱O(填“强”或“弱”).用原子结构解释原因:同主族元素最外层电子数相同,从上到下,电子层数增多,原子半径增大,得电子能力逐渐减弱.
;其水溶液长期在空气中放置容易变浑浊,该变化体现出:S非金属性比O弱O(填“强”或“弱”).用原子结构解释原因:同主族元素最外层电子数相同,从上到下,电子层数增多,原子半径增大,得电子能力逐渐减弱.