题目内容
甲—辛等八种元素在周期表中的相对位置如下表。甲与戊的原子序数相差3,戊的一种单质是自然界硬度最大的物质,丁与辛属同周期元素,下列判断不正确的是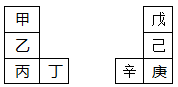
| A.乙的单质在空气中燃烧生成只含离子键的化合物 |
| B.原子半径:辛>己>戊 |
| C.丙与庚的原子核外电子数相差13 |
| D.最高价氧化物的水化物的碱性:丙>乙>甲 |
A
解析试题分析:根据题意可知:甲是Li;乙是Na;丙是K ; 丁是Ca;戊是C,己是Si;庚是Ge;辛是Ga。A.乙的单质在空气中燃烧生成Na2O2是含离子键和非极性共价键的离子化合物,错误;B.题意周期的元素,原子序数越大,原子半径就越小,同一主族的元素,原子核外电子层数越多,原子半径就越大,所以原子半径:辛>己>戊,正确;C.丙是19号元素,庚是32号元素,因此二者的原子核外电子数相差13,正确;D. 同一主族的元素从上到下,元素的金属性逐渐增强,因此最高价氧化物的水化物的碱性就逐渐增强,故最高价氧化物的水化物的碱性:丙>乙>甲,正确。
考点:考查元素的位置、原子结构与元素形成的化合物的性质的关系的知识。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案下列说法正确的是( )
| A.酸雨样品露天放置一段时间,酸性增强,是由于雨水所含成分被氧化的原因 |
| B.CH4、NH3、PH3的热稳定性逐渐增强 |
| C.因为酸性:HC1>HF,所以非金属性:Cl>F |
| D.钠原子在反应中失去的电子比铝原子少,故钠的金属性比铝弱 |
关于元素周期表的说法正确的是( )
| A.元素周期表有8个主族 | B.元素周期表有7个周期 |
| C.短周期是指第一、二周期 | D.IA族的元素全部是金属元素 |
根据表中信息,判断以下叙述正确的是( )
部分短周期元素的原子半径及主要化合价
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.104 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
C.M与T形成的化合物具有两性 D.L2+与R2-的核外电子数相等
已知1—18号元素的离子aW3+、bX+、cY2—、dZ—都具有相同的电子层结构,则下列叙述或表示方法正确的是( )
| A.四种元素位于同一周期 | B.氢化物的稳定性H2Y>HZ |
| C.离子的氧化性aW3+ > bX+ | D.a+3=c﹣2 |
下列各组物质中,酸性由强到弱的排列顺序错误的是
| A.HClO H2CO3 CH3COOH | B.HClO4 HClO3 HClO2 |
| C.HClO4 H2SO4 H3PO4 | D.HClO4 HBrO4 HIO4 |
(原创) 参考消息网6月14日报道:美媒称,中国即将批量生产更为优秀的航空发动机。新发动机将适应更高的内部温度,拥有更出色的性能或耐用性,很可能被安装在作战飞机上,这表明中国工程师已掌握了制造镍基含铼单晶合金叶片的技术(因熵增原理,致成品易含杂质,不易制备)。查资料发现:铼(Re)的熔点3180℃,沸点5627℃;纯铼质软,有良好的机械性能;自然界有2种铼原子 、
、 ,下列说法中正确的是
,下列说法中正确的是
| A.镍基含铼单晶合金属于金属晶体 |
B. 和 和 互称为核素 互称为核素 |
| C.铼(Re)元素的相对原子质量为186 |
| D.含铼合金比纯铼的熔点高、硬度大 |
下列元素的最高价氧化物对应的水化物酸性最强的是
| A.第3周期有7个价电子的元素 |
| B.价电子排布式为3s23p2的元素 |
| C.原子的L电子层p轨道只填了2个电子的元素 |
| D.3p轨道电子半充满的元素 |
X、Y代表两种非金属元素,下列不能说明非金属性X比Y强的是( )
| A.Y的阴离子Y—的还原性强于X的阴离子X— |
| B.X的氢化物的水溶液的酸性比Y的氢化物的水溶液的酸性强 |
| C.X的单质X2能将Y的阴离子Y—氧化成Y2 |
| D.X、Y的单质分别与Fe化合,产物中前者Fe为+3价,后者Fe为+2价 |