题目内容
【题目】已知0.1mol/L的醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是 ( )
CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是 ( )
A.加少量烧碱固体 B.加少量CH3COONa固体
C.加少量冰醋酸 D.加水
【答案】D
【解析】
试题分析:A、加少量烧碱固体,氢氧根离子和氢离子反应,平衡向右移动,醋酸根浓度增大,Ka不变,溶液中c(H+)/c(CH3COOH)值减小,错误;B、加少量CH3COONa固体,醋酸根浓度增大,平衡逆向移动,氢离子浓度减小,醋酸分子浓度增大,溶液中c(H+)/c(CH3COOH)值减小,错误;C、加少量冰醋酸,醋酸的电离程度减小,溶液中c(H+)/c(CH3COOH)值减小,错误;D、加水稀释,醋酸的电离平衡向右移动,溶液中氢离子的物质的量增大,醋酸分子的物质的量减小,溶液体积相同,故溶液中c(H+)/c(CH3COOH)值增大,正确。

 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案 激活思维优加课堂系列答案
激活思维优加课堂系列答案【题目】(平行班做)下表是有机物A、B的有关信息。
A | B |
①能使溴的四氯化碳溶液退色 ②比例模型为: ③能与水在一定条件下反应生成醇 | ①由C、H两种元素组成 ②球棍模型为: |
根据表中信息回答下列问题:
(1)写出A的电子式_____________________。
(2)写出在一定条件下,A生成高分子化合物的化学反应方程式________________________________。
(3)A与氢气发生加成反应后生成分子C,C在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2。当n=_____ 时,这类有机物开始出现同分异构体。
(4)B具有的性质有_____________________(填序号)。
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大
⑤与酸性KMnO4溶液和溴水反应使之退色 ⑥任何条件下不与氢气反应
(5)写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:_____________________________。
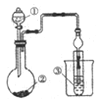
【题目】利用图示装置进行实验,不能得出相应结论的是( )
溶液① | 固体② | 溶液③ | 实验结论 |
| |
A | 稀硫酸 | Na2CO3 | Na2SiO3 | 非金属性:S>C>Si | |
B | 浓盐酸 | KMnO4 | Na2S | 氧化性:KMnO4>Cl2>S | |
C | 浓H2SO4 | Cu | 氢硫酸 | 溶液变浑浊 | |
D | 浓氨水 | CaO | AlCl3 | 可以制备Al(OH)3 |
A. A B. B C. C D. D