题目内容
【题目】下列图示与对应的叙述相符的是
A.如图表示反应2SO2(g)+O2(g)![]() 2SO3(g) ΔH<0在有无催化剂时的能量变化
2SO3(g) ΔH<0在有无催化剂时的能量变化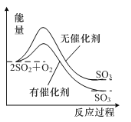
B.如图表示电解精炼铜时纯铜和粗铜的质量随时间的变化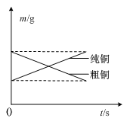
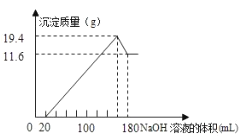
C.如图表示铅蓄电池放电时负极质量随转移电子物质的量的变化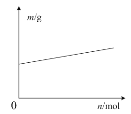
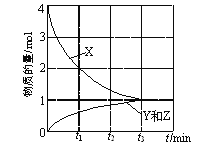
D.如图表示反应2NO2(g)![]() N2O4(g)和2NO2(g)
N2O4(g)和2NO2(g)![]() N2O4(l)的能量变化
N2O4(l)的能量变化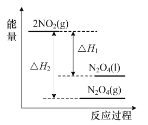
【答案】C
【解析】
A. 催化剂可降低反应的活化能,加快反应速率,但不影响物质本身具有的能量,因此不会改变反应的反应热,A项错误;
B. 电解精炼铜时,阳极溶解的金属除了铜,还有铁、锌等比铜活泼的杂质,阴极只析出金属铜,粗铜溶解减少的质量与纯铜增加的质量不等,B项错误;
C. 铅蓄电池放电时负极的电极反应式为:Pb-2e- + SO42- = PbSO4,生成的PbSO4会附着到负极板上从而使负极板质量增加,则负极质量随转移电子物质的量的增加而增加,C项正确;
D. 物质由气态转为液态时,应放出热量,所以N2O4(g)的能量高于N2O4(l)的能量,D项错误;
故选C。

练习册系列答案
相关题目
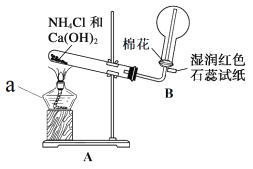
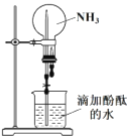
【题目】如图利用培养皿探究氨气的性质,实验时向NaOH固体上滴几滴浓氨水,立即用另一培养皿扣在上面。下表中对实验现象的描述及所做的解释均正确的是
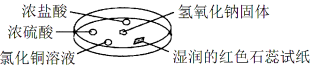
选项 | 实 验 现 象 | 解 释 |
A | 浓盐酸附近产生白烟 | NH3与HCl反应生成了NH4Cl固体 |
B | 浓硫酸附近无明显现象 | NH3与浓硫酸不发生反应 |
C | 氯化铜溶液变白色浑浊 | 白色浑浊的成分是Cu(OH)2 |
D | 湿润的红色石蕊试纸变蓝 | NH3是一种可溶性碱 |