题目内容
【题目】生物质资源是一种污染小的可再生能源,生物质的主要转化途径及主要产物如图。
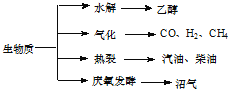
(1)下列有关说法正确的是
A.生物质能,本质上能量来源于太阳能
B.由纤维素水解获得的乙醇属生物质能
C.生物质裂解获得的汽油、柴油等属于纯净物
D.由植物秸秆等发酵获得的沼气,主要成分是甲烷
(2) 由生物质能获得的CO和H2,当两者1: 1催化反应,其原子利用率达100%,合成的物质可能是________。
A.汽油 B.甲醇 C.甲醛(HCHO) D.乙酸
(3) 已知在生物质气化炉中可发生:
C(s)+CO2(g)═2CO(g);△H=+172kJ/mol
CH4(g)+H2O(g)═CO(g)+3H2(g);△H=+206kJ/mol
CH4(g)+2H2O(g)═CO2(g)+4H2(g);△H=+165kJ/mol
则C(s)+H2O(g)═CO(g)+H2(g);△H=____________kJ/mol.
(4)由生物质能获得的CO和H2可以用来合成液态燃料甲醇,实验测得,5g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式:_________________。
(5) 己知稀溶液中,1molH2SO4与NaOH溶液恰好完全反应时,放出114.6kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式_________________。
【答案】(1)abd(3分)(2)cd(2分)(3)+131(kJ/mol)(2分)
(4)CH3OH(l)+![]() O2(g)=CO2(g)+2H2O(l) △H=-726.4kJ/mol(3分)
O2(g)=CO2(g)+2H2O(l) △H=-726.4kJ/mol(3分)
(5)![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)=![]() Na2SO4(aq)+H2O(l) △H=-57.3kJ/mol(3分)
Na2SO4(aq)+H2O(l) △H=-57.3kJ/mol(3分)
【解析】
试题分析:(1)a.生物质本质上能来源于太阳能,故A正确; b.乙醇来源于纤维素,属于生物质能,故B正确;c.汽油、柴油等属于混合物,故C错误;d.沼气的主要成分是甲烷,故D正确;故选abd;
(2))“绿色化学”能实现零排放,即反应物中的原子利用率达到100%,也就是说反应类型一般是化合反应,且反应后产物中的各原子数目比不变,CO和H2在一定条件下按照不同的比例反应,可假定反应时的化学计量数之比为1:1,则只要各选项中的化学式能化为形式(CO)n(H2)n,都是正确的,汽油是混合物,甲醇(CH4O)可变为(CO)1(H2)2,甲醛(CH2O)可变为(CO)1(H2)1,乙酸(C2H4O2)可变为(CO)2(H2)2,故答案为cd;
(3)已知:①C(s)+CO2(g)=2CO(g)△H=172kJ/mol
②CH4(g)+H2O(g)=CO(g)+3H2(g)△H=206kJ/mol
③CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=165kJ/mol
为求C(s)+H2O(g)=CO(g)+H2(g);△H1的反应热,可用盖斯定律将①+③-②可得:
△H=172kJ/mol+165kJ/mol-206kJ/mol=+131kJ/mol;
(4)5gCH3OH在氧气中燃烧生成CO2和液态水,放出113.5kJ热量,64g即1molCH3OH在氧气中燃烧生成CO2和液态水,放出1452.8kJ热量,则热化学方程式为:2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(l)△H=-1452.8KJ;
(5)1molH2SO4溶液与足量 NaOH溶液完全反应,放出114.6kJ的热量,即生成2mol水放出114.6kJ的热量,反应的反应热为-114.6kJ/mol,中和热为-57.3kJ/mol,则中和热的热化学方程式![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)=![]() Na2SO4(aq)+H2O(l) △H=-57.3kJ/mol。
Na2SO4(aq)+H2O(l) △H=-57.3kJ/mol。