题目内容
8.下列反应的离子方程式正确的是( )| A. | 氯化铝与氨水反应:Al3++3OH-═Al(OH)3↓ | |
| B. | 铁与稀盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氯气与水反应:Cl2+H2O?2H++Cl-+ClO- | |
| D. | 向苏打溶液中加入足量的醋酸:CO32-+2CH3COOH═CO2↑+H2O+2CH3COO- |
分析 A.一水合氨为弱电解质,保留化学式;
B.不符合反应客观事实;
C.次氯酸为弱电解质,保留化学式;
D.反应生成醋酸钠、二氧化碳和水.
解答 解:A.氯化铝与氨水反应,离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故A错误;
B.铁与稀盐酸反应生成氯化亚铁和氢气,离子方程式:Fe+2H+═Fe2++H2↑,故B错误;
C.氯气与水反应,离子方程式:Cl2+H2O?H++Cl-+HClO,故C错误;
D.向苏打溶液中加入足量的醋酸,离子方程式:CO32-+2CH3COOH═CO2↑+H2O+2CH3COO-,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质,熟练掌握离子方程式书写方法即可解答,题目难度不大.

练习册系列答案
相关题目
18.A、B、C、D四种元素在周期表中分别处于元素X的四周(如图),已知X元素最高价氧化物的化学式为X2O5,且五种元素中有一种元素的原子半径是它们所处的同族中最小的.试确定:
(1)各元素的符号:A:Si,B:N,C:S,X:P.
(2)画出C元素的简单阴离子的结构示意图: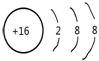
(3)C、D、X最高价氧化物对应水化物酸性由强到弱的顺序:C>X>D(用C、D、X表示).
(4)把A、B、X气态氢化物按照稳定性由强到弱的顺序排列:SiH4<PH3<NH3(用化学式表示).
附加题:A、B、C、D是原子序数小于20的四种元素,已知A元素+1价的阳离子与B、D的阴离子具有相同的电子层结构,B元素最高正价与负价的绝对值之差等于6.1mol C单质与足量的稀硫酸反应可生成1.5mol H2,反应后C元素原子形成的离子和氖原子的电子层结构相同.D元素原子的最外层电子数是C元素原子的最外层电子数的2倍.试回答:
(1)A、B、C、D四种元素依次是钾、氯、铝、硫(写出元素名称).
(2)写出A与C、B与D最高价氧化物的水化物的化学式(按酸性或碱性由强至弱的顺序)碱性:KOH>Al(OH)3,酸性:HClO4>H2SO4.
(3)写出A、C两元素最高价氧化物的水化物间反应的化学方程式Al(OH)3+OH-=AlO2-+2H2O.
| B | ||
| A | X | C |
| D |
(2)画出C元素的简单阴离子的结构示意图:
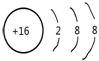
(3)C、D、X最高价氧化物对应水化物酸性由强到弱的顺序:C>X>D(用C、D、X表示).
(4)把A、B、X气态氢化物按照稳定性由强到弱的顺序排列:SiH4<PH3<NH3(用化学式表示).
附加题:A、B、C、D是原子序数小于20的四种元素,已知A元素+1价的阳离子与B、D的阴离子具有相同的电子层结构,B元素最高正价与负价的绝对值之差等于6.1mol C单质与足量的稀硫酸反应可生成1.5mol H2,反应后C元素原子形成的离子和氖原子的电子层结构相同.D元素原子的最外层电子数是C元素原子的最外层电子数的2倍.试回答:
(1)A、B、C、D四种元素依次是钾、氯、铝、硫(写出元素名称).
(2)写出A与C、B与D最高价氧化物的水化物的化学式(按酸性或碱性由强至弱的顺序)碱性:KOH>Al(OH)3,酸性:HClO4>H2SO4.
(3)写出A、C两元素最高价氧化物的水化物间反应的化学方程式Al(OH)3+OH-=AlO2-+2H2O.
3.二氧化硫能使品红褪色,说明二氧化硫具有( )
| A. | 还原性 | B. | 氧化性 | C. | 酸性 | D. | 漂白性 |
13.下列有关物质的用途叙述,错误的是( )
| A. | 碳酸氢钠在医疗上可用于治疗胃酸过多 | |
| B. | 钠和钾的合金常温下是液态,可用于快中子反应堆作热交换剂 | |
| C. | 碳酸钠可用于玻璃,制皂,造纸、纺织等工业 | |
| D. | 氧化钠可用作漂白剂 |
17.常温下不能用于鉴别浓硫酸和稀硫酸的是( )
| A. | 水 | B. | CuSO4晶体 | C. | 铝片 | D. | 铜片 |
1.下列物质中,既能导电,又属于强电解质的一组是( )
| A. | 液态氯化钠、液态氯化氢 | B. | 熔融NaOH、熔融BaSO4 | ||
| C. | 石墨、分析纯盐酸 | D. | 冰醋酸、分析纯硫酸 |
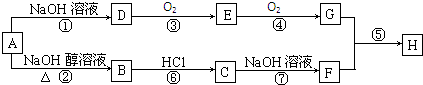
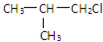 ,G的官能团名称是羧基
,G的官能团名称是羧基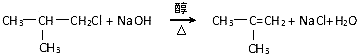 ;E与新制Cu(OH)2反应:
;E与新制Cu(OH)2反应: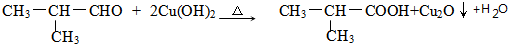 .
.