��Ŀ����
����Ŀ������[CO��NH2��2]�����������˹��ϳɵ��л��
��1����ҵ��������CO2��NH3��һ�������ºϳɣ��䷴Ӧ����ʽΪ_______________��
��2������̼�� ![]() =4��ʱCO2��ת������ʱ��ı仯��ϵ��ͼ1��ʾ��
=4��ʱCO2��ת������ʱ��ı仯��ϵ��ͼ1��ʾ��
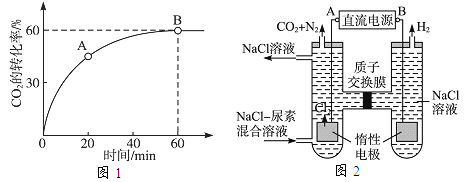
��A����淴Ӧ����v�棨CO2��_______B�������Ӧ����v����CO2������������������������=������
�ڷ�Ӧ�ﵽƽ���NH3��ת����Ϊ_____________��
��3���˹�����ɲ��ü�ӵ绯ѧ������ȥ��л�����е����أ�ԭ����ͼ2��
�ٵ�Դ�ĸ���Ϊ_____������A������B������
���������з����ĵ缫��ӦΪ_________��_________________��
�����������ռ�������13.44L����״���������ȥ������Ϊ________g������������ܽ⣩��
���𰸡� 2NH3+CO2![]() CO��NH2��2+H2O < 30�� B 2Cl--2e-=Cl2�� CO��NH2��2+3Cl2+H2O=N2+CO2+6HCl 7.2
CO��NH2��2+H2O < 30�� B 2Cl--2e-=Cl2�� CO��NH2��2+3Cl2+H2O=N2+CO2+6HCl 7.2
��������(1)CO2��NH3�ϳ�CO(NH2)2�Ļ�ѧ����ʽΪ��2NH3+CO2![]() CO(NH2)2+H2O���ʴ�Ϊ��2NH3+CO2
CO(NH2)2+H2O���ʴ�Ϊ��2NH3+CO2![]() CO(NH2)2+H2O��
CO(NH2)2+H2O��
(2)����CO2��ת������ʱ��仯ͼ��֪����A��ʱ��Ӧ��δ�ﵽƽ��״̬����Ӧ�Խ�����������У���v��(CO2)С��B��ƽ��ʱ�Ļ�ѧ��Ӧ���ʣ��ʴ�Ϊ������
����CO2�ij�ʼ���ʵ���Ϊa����NH3�ij�ʼ���ʵ���Ϊ4a��
2NH3 + CO2![]() CO(NH2)2+H2O
CO(NH2)2+H2O
��ʼ/mol 4a a
ת��/mol 1.2a 0.6a
ƽ��/mol 2.8a 0.4a
ƽ��ʱNH3ת����Ϊ�� ![]() ��100%=30%���ʴ�Ϊ��30%��
��100%=30%���ʴ�Ϊ��30%��
(3)�ٸ��ݵ������������������ŵ���������������ŵ�Ĺ��ɼ�����ͼ�еĵ缫����H2��Cl2�������жϳ�AΪ��Դ��������BΪ��Դ�ĸ������ʴ�Ϊ��B��
���������ȷ���������Ӧ�������������������ط�Ӧ���ɵ�����������̼���Ȼ��⣬�������з����ķ�Ӧ����Ϊ��2Cl--2e-=Cl2����CO(NH2)2+3Cl2+H2O=N2+CO2+6HCl���ʴ�Ϊ��2Cl--2e-=Cl2����CO(NH2)2+3Cl2+H2O=N2+CO2+6HCl��
��������ӦΪ��6H2O+6e-=6OH-+3H2��(��6H++6e-=3H2��)��������ӦΪ��6Cl--6e-=3Cl2����CO(NH2)2+3Cl2+H2O=N2+CO2+6HCl������������Ӧʽ���Կ��������������ϲ�����OH-��H+����Ŀ��ȣ��������з�Ӧ������H+ͨ�����ӽ���Ĥ������������OH-ǡ�÷�Ӧ����ˮ���������е��ǰ����Һ��pH���䣻��������Ӧʽ���Կ�����ת��6mole-ʱ����������3molH2����������1molN2��1molCO2���ʵ���ռ�����13.44 L�����У�V(N2)=V(CO2)= ![]() =2.688L����n(N2)=n(CO2)=0.12 mol�����ݷ���ʽCO(NH2)2+3Cl2+H2O=N2+CO2+6HCl��֪����0.12 mol N2�����ĵ�CO(NH2)2�����ʵ���ҲΪ0.12 mol��������Ϊ��m[CO(NH2)2]=0.12 mol��60 gmol-1=7.2 g���ʴ�Ϊ��7.2��
=2.688L����n(N2)=n(CO2)=0.12 mol�����ݷ���ʽCO(NH2)2+3Cl2+H2O=N2+CO2+6HCl��֪����0.12 mol N2�����ĵ�CO(NH2)2�����ʵ���ҲΪ0.12 mol��������Ϊ��m[CO(NH2)2]=0.12 mol��60 gmol-1=7.2 g���ʴ�Ϊ��7.2��

����Ŀ������ʯ����Ҫ�ɷ�BaCO3����Ca2+��Mg2+��Fe3+�����ʣ���ʵ�������ö���ʯ�Ʊ�BaCl22H2O���������£�
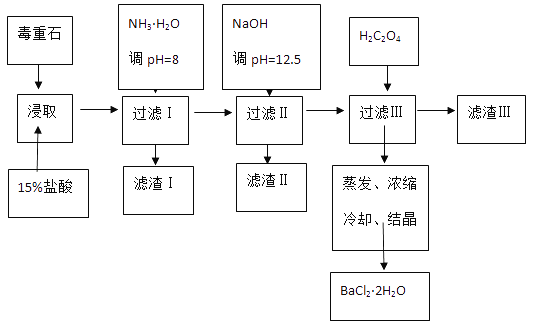
��1��ʵ������37%����������15%�����ᣬ����Ͳ���ʹ�����������е�_________��
a.�ձ� b.����ƿ c.������ d.�ζ���
��2������NH3H2O����pH=8�ɳ�ȥ_______�������ӷ��ţ����������к�________���ѧʽ��������H2C2O4ʱӦ���������ԭ����___________��
Ca2+ | Mg2+ | Fe3+ | |
��ʼ����ʱ��pH | 11.9 | 9.1 | 1.9 |
��ȫ����ʱ��pH | 13.9 | 11.1 | 3.2 |
��BaC2O4����Һ�м���CaCl2���ɷ��������IJ���ת������д����Ӧ�����е����ӷ���ʽ___________________������÷�Ӧ��ƽ�ⳣ��K=___________��Ksp��BaC2O4��=1.6��10-7��Ksp��CaC2O4��=2.3��10-9������һλС����
��3�����ü�����ζ����ɲⶨBa2+�ĺ�����ʵ����������С���֪��2CrO42-+2H+=Cr2O72-+H2O Ba2++CrO42-=BaCrO4��
���������ƶ�x mLһ��Ũ�ȵ�Na2CrO4��Һ����ƿ�У��������ָʾ������b molL-1�����Һ�ζ����յ㣬��õμ��������ΪV0mL��
����������ȡy mL BaCl2��Һ����ƿ�У�����x mL�벽������ͬŨ�ȵ�Na2CrO4��Һ����Ba2+��ȫ�������ټ������ָʾ������b molL-1�����Һ�ζ����յ㣬��õμ���������ΪV1mL�������������ݣ��ɼ����BaCl2��ҺŨ��Ϊ_________molL-1���ú���ĸ��ʽ�ӱ�ʾ�������������еμ�����ʱ����������Һ��������Ba2+Ũ�ȵIJ���ֵ��_______������ƫ��������ƫС������
����Ŀ���������ʵķ����������ȷ����
A | B | C | D | |
ǿ����� | Cu(OH)2 | KCl | HCl | CaCO3 |
������� | NaOH | NH3H2O | BaSO4 | CH3COOH |
�ǵ���� | SO2 | ���ʯ | NH3 | C2H5OH |
�������� | ʯī | ϡH2SO4 | ����KCl | ͭ |
A. A B. B C. C D. D