题目内容
硝酸盐受热分解的产物与硝酸盐的组成以及受热的温度等因素有关。
Ⅰ.一定条件下硝酸铵受热分解的化学反应方程式为:NH4NO3→HNO3+N2 +H2O(未配平)
(1)该反应中发生还原反应的过程是_______→________。
(2)反应中被氧化与被还原的氮原子数之比为__________;现有1mol NH4NO3分解,生成的氧化产物的物质的量是 mol。
Ⅱ.硝酸铵受撞击或高温发生爆炸的化学反应方程式为:m NH4NO3→n O2+p N2+q H2O
(3)下列关于该方程式中化学计量数的说法正确的是_________(选填字母编号)。
a.m=1 b.n=2 c.p=3 d.q=4
(4)若反应过程中共转移3.01×1023个电子,则反应可产生气体的体积为_____(标准状况)。
Ⅰ.一定条件下硝酸铵受热分解的化学反应方程式为:NH4NO3→HNO3+N2 +H2O(未配平)
(1)该反应中发生还原反应的过程是_______→________。
(2)反应中被氧化与被还原的氮原子数之比为__________;现有1mol NH4NO3分解,生成的氧化产物的物质的量是 mol。
Ⅱ.硝酸铵受撞击或高温发生爆炸的化学反应方程式为:m NH4NO3→n O2+p N2+q H2O
(3)下列关于该方程式中化学计量数的说法正确的是_________(选填字母编号)。
a.m=1 b.n=2 c.p=3 d.q=4
(4)若反应过程中共转移3.01×1023个电子,则反应可产生气体的体积为_____(标准状况)。
(1)NH4NO3→N2 (1分1格,共2分)
(2)5∶3; 0.5 (1分1格,共2分)
(3)d (2分)
(4)3.36 L(2分)
试题分析:(2)5NH4NO3= 2HNO3+4N2 +9H2O 5N-3 ----5N0 被氧化的氮原子为5;3N+5----3N0 被还原的氮原子为3;被氧化与被还原的氮原子数之比为5∶3;1mol NH4NO3生成的氧化产物为0.5 mol N2.
(3)2NH4NO3→ O2+2 N2+4 H2O m=2 n=1 p=2 q=4 符合的是d.
(4)解:设O2的物质的量为n
2NH4NO3→ O2→2 N2→4 H2O→10e-
1 2 10* 6.02×1023
n 2n 3.01×1023
n=0.05 (n+2n)*22.4=3*0.05*22.4= 3.36(L)

练习册系列答案
相关题目
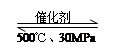 2NH3(g)△H=-38.6kJ·mol-1
2NH3(g)△H=-38.6kJ·mol-1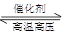 2NH3(g)△H﹤0,升高温度,可使反应速率增大,反应逆向移动
2NH3(g)△H﹤0,升高温度,可使反应速率增大,反应逆向移动