题目内容
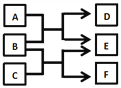
【题目】X、Y、Z、W是原子序数依次增大的四种短周期元素,A、B、C、D、F是由其中的两种或三种元素组成的化合物,E是由Z元素形成的单质,0.1molL-1 D溶液的pH为13(25℃)。它们满足如图转化关系,则下列说法正确的是
A. 由X、Y、Z、W四种元素组成的盐溶液pH小于7
B. 化合物F中含有共价键和离子键
C. 0.1molB与足量C完全反应共转移电子数为0.2NA
D. Z元素的最高正价为+6
【答案】B
【解析】X、Y、Z、W是原子序数依次增大的四种短周期元素,A、B、C、D、F是由其中的两种或三种元素组成的化合物,E是由Z元素形成的单质,0.1molL-1D溶液的pH为13(25℃),则D溶液为一元强碱溶液,且其中的金属元素在短周期,则金属元素为Na元素,所以D是NaOH,A和B反应生成强碱,且A和B都是化合物,E是单质,则该反应是过氧化钠和水的反应,所以E是O2,则Z元素是O元素,W的原子序数大于Z,所以W是Na元素;B和C反应生成氧气,两种化合物反应生成氧气的还有过氧化钠和二氧化碳的反应,所以B是Na2O2,则A是H2O,C是CO2,F是Na2CO3,X的原子序数小于Y,则X是H元素,Y是C元素,即X是H、Y是C、Z是O、W是Na元素,A.由X、Y、Z、W四种元素组成的盐是碳酸氢钠,其溶液pH大于7,A错误;B.化合物F是Na2CO3,碳酸钠中钠离子和碳酸根离子之间存在离子键、C原子和O原子之间存在共价键,所以碳酸钠中含有共价键和离子键,B正确;C.B是Na2O2,C是CO2,在B和C的反应中,氧化剂和还原剂都是过氧化钠,0.1molB与足量C完全反应共转移电子数为0.1NA,C错误;D.Z是O元素,其没有正化合价,D错误;答案选B。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目