题目内容
【题目】在一定条件下,可逆反应:N2(g)+3H2(g)![]() 2NH3(g) △H<0达到平衡,当单独改变下列条件后,有关叙述错误的是( )
2NH3(g) △H<0达到平衡,当单独改变下列条件后,有关叙述错误的是( )
A.加催化剂, v(正)v(逆)都发生变化,而且变化的倍数相等
B.加压, v(正)v(逆)都增大,且v(正)增大的倍数大于v(逆)增大的倍数
C.升温, v(正)v(逆)都增大,且v(正)增大的倍数大于v(逆)增大的倍数
D.加入氩气,v(正)v(逆)都不变,且v(正)等于v(逆)
【答案】C
【解析】
A.加入催化剂,正逆反应速率都增大,且增大的倍数相同,平衡不移动,故A正确;
B.反应物气体的化学计量数大于生成物气体的化学计量数,增大压强,v(正)、v(逆)都增大,平衡向正反应方向移动,说明v(正)增大的倍数大于v(逆)增大的倍数,故B正确;
C.正反应放热,则升高温度平衡向逆反应方向移动,正逆反应速率都增大,v(正)增大的倍数小于v(逆)增大的倍数,故C错误;
D.在体积不变的密闭容器中通入氩气,虽然压强增大,但参加反应的气体的浓度不变,反应速率不变,平衡不移动,即v(正)v(逆)都不变,且v(正)仍等于v(逆),故D正确;
故答案为C。

【题目】某温度下,反应H2(g)+CO2(g)![]() H2O(g)+CO(g)的平衡常数K=
H2O(g)+CO(g)的平衡常数K=![]() 。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示:
。该温度下,在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示:
甲 | 乙 | 丙 | |
c(H2)/(mol·L-1) | 0.010 | 0.020 | 0.020 |
c(CO2)/(mol·L-1) | 0.010 | 0.010 | 0.020 |
下列判断不正确的是( )
A. 反应开始时,丙容器中化学反应速率最大,甲容器中化学反应速率最小
B. 平衡时,乙容器中CO2的转化率大于60%
C. 平衡时,甲容器中和丙容器中H2的转化率均是60%
D. 平衡时,丙容器中c(CO2)是甲容器中的2倍,是 0.012 mol·L-1
【题目】某学生用0.2000mol/L的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体 ③调节液面至“0”或“0”刻度线以下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数。 请回答:
⑴以上步骤有错误的是(填编号)______,该错误操作会导致测定结果(填“偏大”、“偏小”或“无影响”)________
⑵下列选项将导致测定结果偏小的是___________
A.步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡
B.滴定到终点读数时,仰视滴定管的刻度,其他操作正确
C.盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗
D.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液
⑶判断滴定终点的现象是:__________________________________________________________
⑷下图是某次滴定时的滴定管中的液面,其读数为 ___________mL
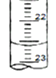
⑸根据下列数据:请计算待测盐酸溶液的浓度:__________mol/L
滴定次数 | 待测体积(ml) | 标准烧碱体积(ml) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.40 | 20.40 |
第二次 | 20.00 | 4.00 | 24.00 |
第三次 | 20.00 | 2.00 | 24.10 |