题目内容
14.甲烷是一种重要的化工原料,以甲烷为主要原料合成D(一种重要的有机合成中间体)的路线如图.请回答下列问题: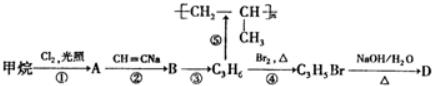
(1)反应⑤的反应类型为加聚反应;反应③的条件为催化剂.
(2)D的结构简式为CH2=CHCH2OH.
(3)反应②的化学方程式为CH3Cl+CH≡CNa→CH2=CCH3+NaCl.
(4)反应④的化学方程式为CH2=CHCH3+Br2$\stackrel{△}{→}$CH2=CHCH2Br+HBr.
(5)请设计一个实验,证明D中含有碳碳双键官能团用试管量取一定量的D,向试管中加入少量溴的四氯化碳溶液,若褪色,就说明含有碳碳双键.
分析 甲烷发生取代反应生成A,A和乙炔钠反应生成B,根据反应⑤知,C3H6结构简式为CH2=CHCH3,A和乙炔钠发生取代反应生成B为CH≡CCH3,B发生加成反应生成CH2=CHCH3,A为CH3Cl;
丙烯和溴发生取代反应生成CH2=CHCH2Br,CH2=CHCH2Br发生取代反应生成D为CH2=CHCH2OH,据此分析解答.
解答 解:甲烷发生取代反应生成A,A和乙炔钠反应生成B,根据反应⑤知,C3H6结构简式为CH2=CHCH3,A和乙炔钠发生取代反应生成B为CH≡CCH3,B发生加成反应生成CH2=CHCH3,A为CH3Cl;丙烯和溴发生取代反应生成CH2=CHCH2Br,CH2=CHCH2Br发生取代反应生成D为CH2=CHCH2OH,
(1)反应⑤的反应类型为加聚反应;反应③为加成反应,需要的条件为催化剂,
故答案为:加聚反应;催化剂;
(2)D的结构简式为CH2=CHCH2OH,故答案为:CH2=CHCH2OH;
(3)反应②为一氯甲烷和乙炔钠的取代反应,反应方程式为CH3Cl+CH≡CNa→CH2=CCH3+NaCl,
故答案为:CH3Cl+CH≡CNa→CH2=CCH3+NaCl;
(4)反应④为丙烯的取代反应,反应方程式为CH2=CHCH3+Br2$\stackrel{△}{→}$CH2=CHCH2Br+HBr,
故答案为:CH2=CHCH3+Br2$\stackrel{△}{→}$CH2=CHCH2Br+HBr;
(5)D为丙烯醇,碳碳双键能和溴发生加成反应而使溴的四氯化碳溶液褪色,所以可以用溴的四氯化碳溶液检验,其检验方法是:用试管量取一定量的D,向试管中加入少量溴的四氯化碳溶液,若褪色,就说明含有碳碳双键,故答案为:用试管量取一定量的D,向试管中加入少量溴的四氯化碳溶液,若褪色,就说明含有碳碳双键.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,注意烯烃和溴没有条件时发生加成反应,在加热条件下发生取代反应,为易错点.

| A. | 向FeCl2溶液中滴加少量KSCN溶液变血红色,说明FeCl2完全被氧化成FeCl3 | |
| B. | 相同条件下,Na2CO3溶液的碱性强于C6H5ONa,说明C6H5OH的酸性强于H2CO3 | |
| C. | 向漂白粉上加入较浓的盐酸,产生的气体不能使湿润淀粉碘化钾试纸变蓝,说明该漂白粉已经失效 | |
| D. | 向浓度均为0.1 mol•L-1 NaCl 和NaI 混合溶液中滴加少量AgNO3溶液,产生黄色沉淀,说明Ksp(AgCl)<Ksp(AgI) |
| A. | 淀粉-碘化钾溶液和溴水 | B. | 氢氧化钠溶液与碘水 | ||
| C. | 新制Cu(OH)2悬浊液与碘水 | D. | 碘化钾溶液与碘水 |
| A. | 各加入2.3g | B. | 各加入0.1mol | C. | 各加入0.01mol | D. | 各加入0.23g |
| A. | 乙烯的比例模型: | |
| B. | 甲基的电子式: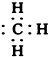 | |
| C. | 乙醇的最简式:C2H6O | |
| D. | 中子数为53、质子数为78的碘原子:${\;}_{53}^{111}$I |
| A. | 硫酸铜溶液与氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ | |
| B. | 将大理石投入到足量盐酸中:CO32-+2H+═CO2↑+H2O | |
| C. | 将Cl2通入KI溶液中:2I-+Cl2═2Cl-+I2 | |
| D. | 硫酸镁溶液和氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ |
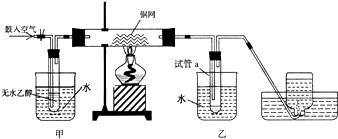
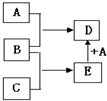 已知A、B、C均为常见单质,其中A是金属,B、C是非金属,在一定条件下相互转化关系如图所示(反应条件和部分产物已省略).
已知A、B、C均为常见单质,其中A是金属,B、C是非金属,在一定条件下相互转化关系如图所示(反应条件和部分产物已省略). ,A和E在一定条件下反应生成D的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO.
,A和E在一定条件下反应生成D的化学方程式为2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO.