题目内容
12.高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝、助凝、杀菌、除臭为一体的新型高效多功能绿色水处理剂,具有良好的应用前景.其生产工艺如下: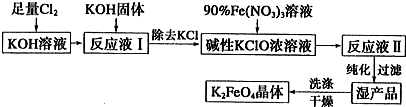
已知:①2KOH+Cl2═KCl+KClO+H2O(条件:温度较低)
②6KOH+3C12═5KCl+KClO3+3H2O(条件:温度较高)
回答下列问题:
(1)该生产工艺应在温度较低(填“温度较高’’或“温度较低”)的情况下进行.
(2)写出Fe(NO3)3在强碱性条件下与KClO反应制K2FeO4的离子方程式2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O.
(3)在“反应液I”中加KOH固体的目的是AC(填序号).
A.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
B.KOH固体溶解时会放出较多的热量,有利于提高反应速率
C.为下一步反应提供反应物 D.使副产物KClO3化为KClO.
分析 足量氯气通入氢氧化钾溶液中低温反应生成次氯酸钾、氯化钾和水,加入固体氢氧化钾除去氯化钾得到减小次氯酸钾浓溶液,加入硝酸铁浓溶液纯化洗涤干燥得到高铁酸钾,
(1)由工艺流程及③可知,利用Fe(NO3)3与KClO制备K2FeO4,由信息②可知温度较高KOH与Cl2 反应生成的是KClO3;
(2)根据题目信息、氧化还原反应中化合价发生变化确定产物以及电子得失守恒和质量守恒来配平;
(3)根据生产工艺流程图,第①步氯气过量,第③步需要碱性条件,在温度较高时KOH 与Cl2 反应生成的是KClO3,氧化还原反应中化合价有升有降.
解答 解:足量氯气通入氢氧化钾溶液中低温反应生成次氯酸钾、氯化钾和水,加入固体氢氧化钾除去氯化钾得到减小次氯酸钾浓溶液,加入硝酸铁浓溶液纯化洗涤干燥得到高铁酸钾,
(1)由工艺流程及③可知,利用Fe(NO3)3与KClO制备K2FeO4,由信息②可知温度较高KOH与Cl2 反应生成的是KClO3.由信息①可知,在低温下KOH与Cl2 反应生成的是KClO,故选择低温较低,
故答案为:温度较低;
(2)据题目信息和氧化还原反应中化合价发生变化确定找出反应物:Fe3+、ClO-,生成物:FeO42-、Cl-,根据电子得失守恒和质量守恒来配平,可得2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O,
故答案为:2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O;
(3)A、根据生产工艺流程图,第①步氯气过量,加入KOH固体后会继续反应生成KClO,故A正确;
B、因温度较高时KOH 与Cl2 反应生成的是KClO3,而不是KClO,故B错误;
C、第③步需要碱性条件,所以碱要过量,故C正确;
D、KClO3转化为 KClO,化合价只降不升,故D错误;
故选:AC.
点评 本题结合高铁酸钾(K2FeO4)的制备主要考查了氧化还原反应的知识、离子的检验等,培养了学生运用知识的能力,题目难度中等.

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案| 选项 | 实验目的 | 实验目的或结论 |
| A | 向含有少量FeCl2的MgCl2溶液中加入足量NaOH溶液,搅拌后静置过滤 | 除去MgCl2溶液中少量FeCl2 |
| B |  | NaHCO3比Na2CO3受热更易分解 |
| C | 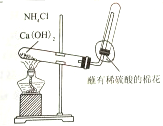 | 制取并收集氨气 |
| D | 将混有Ca(OH)2杂质的Mg(OH)2样品,放入水中搅拌成浆状后,加入足量饱和氯化镁溶液充分搅拌,过滤,沉淀用蒸馏水洗涤 | 除去Mg(OH)2样品中Ca(OH)2 |
| A. | A | B. | B | C. | C | D. | D |
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
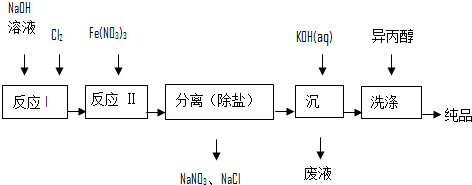
①洗涤粗品时选用异丙醇而不用水的理由是:减少高铁酸钾的溶解损失.
②反应Ⅰ的离子方程式为Cl2+20H-=Cl-+ClO-+H2O.
③反应Ⅱ中氧化剂与还原剂之比为3:2.
④已知25℃时Fe(OH)3的Ksp=4.0×10-38,反应Ⅱ后的溶液中c(Fe3+)=4.0×10-5 mol/L,则需要调整pH=3时,开始生成Fe(OH)3(不考虑溶液体积的变化).
(2)由流程图可见,湿法制备高铁酸钾时,需先制得高铁酸钠,然后再向高铁酸钠中加入饱和KOH溶液,即可析出高铁酸钾.
①加入饱和KOH溶液的目的是:增大K+浓度,促进高铁酸钾晶体析出.
②由以上信息可知:高铁酸钾的溶解度比高铁酸钠小(填“大”或“小”).
(3)请写出干法制备K2FeO4的化学反应方程式Fe2O3+3KNO3+4KOH=2K2FeO4+3KNO2+2H2O.
| A. | 反应在tmin内的平均速率为v(D)=0.4/tmol•L-1•min-1 | |
| B. | 温度升至500℃时,上述反应平衡常数为0.64,则正反应为吸热反应 | |
| C. | 保持其他条件不变,向平衡体系中再通入0.2molB,与原平衡相比,达到新平衡时A转化率增大,B的体积分数增大 | |
| D. | 若反应开始时向密闭容器中充入2.4mol 的A和1.2mol 的B,达到平衡所需时间小于t |
| A. | 开发新能源,如太阳能、风能等,减少对化石能源的依赖 | |
| B. | 直径接近于2.5×10-6m的颗粒物(PM2.5)分散在空气中形成的混合物具有丁达尔效应 | |
| C. | 燃煤进行脱硫、脱硝处理,减少硫氧化物和氮氧化物的排放 | |
| D. | 通过吸收空气中CO2并利用廉价能源合成汽油可推广“绿色自由”计划 |
 谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是____ __。
谨,该组同学在2mLFeCl2溶液中先加入0.5mL煤油,再于液面下依次加入几滴氯水和l滴KSCN溶液,溶液变红,煤油的作用是____ __。 SCN溶液,溶
SCN溶液,溶