题目内容
3.科学家冶炼出了纯度高达99.9999%的铁,你估计它不会具有的性质是( )| A. | 在潮湿的空气中放置不易生锈 | B. | 硬度比生铁大 | ||
| C. | 与2mol/L盐酸的反应生成氢气 | D. | 在冷的浓H2SO4溶液中可钝化 |
分析 A.纯铁不能形成原电池;
B.合金的硬度比各成分金属的大;
C.铁在金属活动顺序表中排在氢的前面;
D.铁铝在冷的浓硫酸中可以钝化.
解答 解:A.纯铁不能形成原电池,在潮湿的空气中不易生锈,故A正确;
B.生铁是合金,硬度比纯铁大,故B错误;
C.铁在金属活动顺序表中排在氢的前面,能和盐酸反应生成氯化亚铁和氢气,故C正确;
D.铁在冷的浓硫酸中可以钝化,故D正确.
故选C.
点评 本题考查合金的性质、原电池等,难度不大,注意原电池能加快化学反应速率.

练习册系列答案
相关题目
6. 某无色稀溶液X中,可能含有下表所列离子中的某几种.
某无色稀溶液X中,可能含有下表所列离子中的某几种.
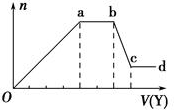
现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系图所示.(提示:铵根和偏铝酸根不能共存)
(1)若Y是盐酸,则X溶液中一定含有的离子是SiO32-、AlO2-、CO32-、Na+,ab段发生反应的总离子方程式为CO32-+2H+=H2O+CO2↑,图中Oa段与Y溶液反应的离子的物质的量之比为【要标明离子符号,如n(Na+)】.
(2)若Y是NaOH溶液,则ab段反应的离子方程式为NH4++OH-═NH3•H2O; bc段反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.若不考虑离子的水解因素,忽略H+和OH-,且溶液中只存在4种离子,则它们的离子个数比为【要标明离子符号,如n(Na+),按阳离子在前,阴离子在后,高价在前,低价在后得顺序排列】.
 某无色稀溶液X中,可能含有下表所列离子中的某几种.
某无色稀溶液X中,可能含有下表所列离子中的某几种.| 阴离子 | CO32-、SiO32-、AlO2-、Cl- |
| 阳离子 | Al3+、Fe3+、Mg2+、NH4+、Na+ |
(1)若Y是盐酸,则X溶液中一定含有的离子是SiO32-、AlO2-、CO32-、Na+,ab段发生反应的总离子方程式为CO32-+2H+=H2O+CO2↑,图中Oa段与Y溶液反应的离子的物质的量之比为【要标明离子符号,如n(Na+)】.
(2)若Y是NaOH溶液,则ab段反应的离子方程式为NH4++OH-═NH3•H2O; bc段反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.若不考虑离子的水解因素,忽略H+和OH-,且溶液中只存在4种离子,则它们的离子个数比为【要标明离子符号,如n(Na+),按阳离子在前,阴离子在后,高价在前,低价在后得顺序排列】.
11.下列装置是从废溴化铝催化剂中制取单质溴并回收氯化铝实验的部分装置,不能达到实验目的是( )
| A. |  用图所示装置氧化Br- | |
| B. | 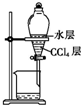 用图所示装置萃取Br2 | |
| C. | 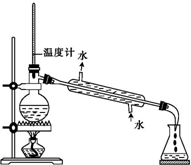 用图所示装置分离CCl4和Br2 | |
| D. |  用图所示的装置将含AlCl3的溶液蒸发制取无水AlCl3 |
18.能鉴别SO2和CO2的试剂是( )
| A. | 品红溶液 | B. | 澄清石灰水 | C. | 紫色石蕊试液 | D. | 高锰酸钾溶液 |
15.将a mol的NH3与b mol的O2混合后,充入一密闭容器,在Pt存在下升温至700℃,充分反应后,冷却至室温.
(1)请讨论b∕a的取值范围及与之对应的溶液的溶质及其物质的量,将结果填于下表中:
(2)当a=2.00,b=4.00,在室温下得到的产物是什么?若该产物的密度为1.44g.ml-1,则其溶质的质量分数和物质的量浓度各是多少?
(1)请讨论b∕a的取值范围及与之对应的溶液的溶质及其物质的量,将结果填于下表中:
| b∕a的取值范围 | 溶质 | 溶质物质的量 |
12.把2.1g CO与H2组成的混合气体与足量的O2充分燃烧后,立即将产物全部通入到足量的Na2O2固体中,则固体的质量增加了( )
| A. | 2.1 g | B. | 3.6 g | C. | 7.2 g | D. | 无法确定 |
13.为了确定(NH4)2Fe(SO4)2•6H2O(硫酸亚铁铵晶体)的成分,下列实验操作及叙述中不正确的是( )
| A. | 取少量样品放入试管中,加热,试管口放一团蘸有无水硫酸铜粉末的棉花团,变蓝则可证明晶体的成分中含有结晶水 | |
| B. | 取少量样品溶于水,向溶液中滴入几滴新制氯水,再滴入2滴KSCN溶液,溶液变为红色,则可证明晶体的成分中含有Fe2+ | |
| C. | 取少量样品溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42- | |
| D. | 取少量样品放入试管中,加入少量浓NaOH溶液并加热,在试管口用湿润的红色石蕊试纸检验,则可证明晶体的成分中是否含有NH4+ |