题目内容
18.某实验小组用如图所示装置进行乙醇的催化氧化实验.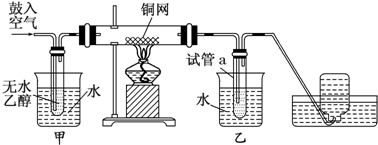
(1)实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO、CuO+CH3CH2OH$\stackrel{△}{→}$CH3CHO+Cu+H2O.
(2)装置中有甲和乙两个水浴:甲的作用是加热;乙的作用是冷却.
(3)反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是乙醛、乙醇、水,集气瓶中收集到的主要成分是氮气、氧气.
分析 设计乙醇的催化氧化实验,由图中装置可知,利用空气将无水乙醇蒸气赶入有铜网的试管中,加热下大试管中发生2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO、CuO+CH3CH2OH$\stackrel{△}{→}$CH3CHO+Cu+H2O,在乙中冷水冷却使蒸气转化为液体,最后排水法收集到空气中不溶于水的气体,以此来解答.
解答 解:(1)实验过程中铜网出现红色和黑色交替的现象,相应的化学方程式为2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO、CuO+CH3CH2OH$\stackrel{△}{→}$CH3CHO+Cu+H2O
故答案为:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO、CuO+CH3CH2OH$\stackrel{△}{→}$CH3CHO+Cu+H2O;
(2)装置中有甲和乙两个水浴:甲的作用是加热,使乙醇转化为气体,乙的作用是冷却,使反应产物转化为液体,故答案为:加热;冷却;
(3)反应进行一段时间后,发生CuO+CH3CH2OH$\stackrel{△}{→}$CH3CHO+Cu+H2O,冷却后在干燥试管a中能收集到不同的物质为乙醛、乙醇、水,空气中氧气、氮气不溶于水,则排水法收集到氮气、氧气,故答案为:乙醛、乙醇、水;氮气、氧气.
点评 本题考查性质实验方案的设计,为高频考点,把握有机物的性质、实验装置的作用、实验设计意图等为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
9.下列推断正确的是( )
| A. | SiO2 是酸性氧化物,不溶于水,也不能与任何酸发生反应 | |
| B. | Na2O、Na2O2组成元素虽然相同,但与H2O、CO2等反应的产物不完全相同 | |
| C. | CO、SO2、NO、NO2都是对大气产生污染的气体,他们在空气中都能稳定存在 | |
| D. | 浓硫酸可用于干燥氢气、氯化氢、碘化氢等气体,但不能干燥氨气、二氧化氮气体 |
6.开发新型储氢材料是氢能利用的重要研究方向.
Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
(1)基态Ti3+的未成对电子数有1个.
(2)LiBH4由Li+和BH4-构成,LiBH4中不存在的作用力有C(填标号).
A.离子键 B.共价键 C.金属键 D.配位键
(3)Li、B、H元素的电负性由大到小排列顺序为H>B>Li.
(4)分子X可以通过氢键形成“笼状结构”而成为潜在的储氢材料.X一定不是BC(填标号).
A.H2O B.CH4 C.HF D.CO(NH2)2
(5)钾、镁、氟形成的某化合物的晶体结构为K+在立方晶胞的中心,Mg2+在晶胞的8个顶角,F-处于晶胞的棱边中心.由钾、镁、氟形成的该化合物的化学式为KMgF3,每个K+与12个F-配位.
(6)判断含氧酸酸性强弱的一条经验规律是含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强.如下表所示:含氧酸酸性强弱与非羟基氧原子数的关系
亚磷酸H3PO3和亚砷酸H3AsO3分子式相似,但它们的酸性差别很大,H3PO3是中强酸,H3AsO3既有弱酸性又有弱碱性.由此可推出H3AsO3结构式为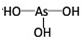 .H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:
.H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:
①H3PO3+2NaOH=Na2HPO3+2H2O,
②H3AsO3+3NaOH=Na3AsO3+3H2O.
Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得.
(1)基态Ti3+的未成对电子数有1个.
(2)LiBH4由Li+和BH4-构成,LiBH4中不存在的作用力有C(填标号).
A.离子键 B.共价键 C.金属键 D.配位键
(3)Li、B、H元素的电负性由大到小排列顺序为H>B>Li.
(4)分子X可以通过氢键形成“笼状结构”而成为潜在的储氢材料.X一定不是BC(填标号).
A.H2O B.CH4 C.HF D.CO(NH2)2
(5)钾、镁、氟形成的某化合物的晶体结构为K+在立方晶胞的中心,Mg2+在晶胞的8个顶角,F-处于晶胞的棱边中心.由钾、镁、氟形成的该化合物的化学式为KMgF3,每个K+与12个F-配位.
(6)判断含氧酸酸性强弱的一条经验规律是含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强.如下表所示:含氧酸酸性强弱与非羟基氧原子数的关系
| 次氯酸 | 磷酸 | 硫酸 | 高氯酸 | |
| 含氧酸 | Cl-OH | 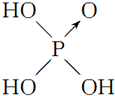 |  | 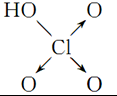 |
| 非羟基氧原子数 | 0 | 1 | 2 | 3 |
| 酸性 | 弱酸 | 中强酸 | 强酸 | 最强酸 |
 .H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:
.H3PO3和H3AsO3与过量的NaOH溶液反应的化学方程式分别是:①H3PO3+2NaOH=Na2HPO3+2H2O,
②H3AsO3+3NaOH=Na3AsO3+3H2O.
13.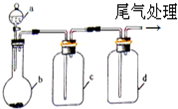 实验室中某些气体的制取、除杂及收集装置如图所示.仅用此装置和表中提供的物质完成相关实验,最合理的是( )
实验室中某些气体的制取、除杂及收集装置如图所示.仅用此装置和表中提供的物质完成相关实验,最合理的是( )
 实验室中某些气体的制取、除杂及收集装置如图所示.仅用此装置和表中提供的物质完成相关实验,最合理的是( )
实验室中某些气体的制取、除杂及收集装置如图所示.仅用此装置和表中提供的物质完成相关实验,最合理的是( )| 选项 | a中物质 | b中物质 | c中物质 | d中收集的气体 |
| A | 浓氨水 | CaO | 浓H2SO4 | NH3 |
| B | 浓盐酸 | MnO2 | 饱和NaCl溶液 | Cl2 |
| C | 饱和食盐水 | Na2O2 | CuSO4溶液 | O2 |
| D | 浓硫酸 | Na2SO3 | 浓H2SO4 | SO2 |
| A. | A | B. | B | C. | C | D. | D |
7.某研究小组通过实验探究Cu及其化合物的性质,操作正确且能达到目的是( )
| A. | 将铜丝插入浓硫酸加热,反应后把水加入反应器中,观察硫酸铜溶液的颜色 | |
| B. | 常温下将铜丝伸入盛满氯气的集气瓶中,观察CuCl2的生成 | |
| C. | 金属钠放入硫酸铜溶液中可以置换出金属铜 | |
| D. | 将表面有铜绿[Cu2(OH)2CO3]的铜器放入盐酸中浸泡,除去铜绿 |
8.下列说法不正确的是( )
| A. | 常温下,醋酸钠与醋酸的混合溶液pH=7,c(Na+)=c(CH3COO-) | |
| B. | 0.1 mol/L Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) | |
| C. | 常温下,将pH=1的醋酸溶液稀释100倍后,水电离的c(H+)=10-11mol/L | |
| D. | 0.1mol/L NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-) |
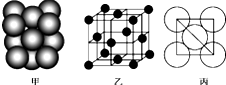 铜单质晶体中原子的堆积方式如图甲所示,其晶胞如图乙所示,原子之间相互位置关系的平面图如图丙所示.
铜单质晶体中原子的堆积方式如图甲所示,其晶胞如图乙所示,原子之间相互位置关系的平面图如图丙所示. “神七”登天标志着我国的航天事业进入了新的篇章.
“神七”登天标志着我国的航天事业进入了新的篇章.