题目内容
【题目】下列条件下,两瓶气体所含原子数一定相等的是( )
A.同温度、同体积的H2和N2B.同体积、同密度的C2H4和CH4
C.同质量、不同密度的N2和COD.同压强、同体积的N2O和CO2
【答案】C
【解析】
A. 气体体积受温度、压强的影响,同温、同体积的H2和N2,因为压强未知,所以两种气体的物质的量不一定相同,所含分子数不一定相同,导致所含原子数不一定相同,故A错误;
B. 同体积同密度的C2H4和CH4,两种气体的质量相同,由N=n×NA=![]() ×NA,设C2H4和CH4均为ag,计算可知同体积、同密度的C2H4所含原子物质的量为:
×NA,设C2H4和CH4均为ag,计算可知同体积、同密度的C2H4所含原子物质的量为:![]() ,CH4所含原子物质的量为:
,CH4所含原子物质的量为:![]() ,故B错误;
,故B错误;
C. 两种气体的质量相同,摩尔质量相同,则所含分子数相同,且氮气和一氧化碳都是双原子分子,所以含有的原子数相同,故C正确;
D. 气体体积受温度、压强的影响,因为温度未知,所以同压、同体积的N2O和CO2,两种气体的物质的量不一定相等,所含分子数不一定相等,导致所含原子数不一定相等,故D错误;
故选C。

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案【题目】CO2和CO可作为工业合成甲醇(CH3OH)的直接碳源,还可利用CO2据电化学原理制备塑料,既减少工业生产对乙烯的依赖,又达到减少CO2排放的目的。
(1)利用CO2和H2反应合成甲醇的原理为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。
CH3OH(g)+H2O(g)。
上述反应常用CuO和ZnO的混合物作催化剂。相同的温度和时间段内,催化剂中CuO的质量分数对CO2的转化率和CH3OH的产率影响的实验数据如下表所示:
ω(CuO)/% | 10 | 20 | 30 | 4b | 50 | 60 | 70 | 80 | 90 |
CH3OH的产率 | 25% | 30% | 35% | 45% | 50% | 65% | 55% | 53% | 50% |
CO2的转化率 | 10% | 13% | 15% | 20% | 35% | 45% | 40% | 35% | 30% |
由表可知,CuO的质量分数为________催化效果最佳。
(2)利用CO和H2在一定条件下可合成甲醇,发生如下反应:CO(g)+2H2(g)![]() CH3OH(g),其两种反应过程中能量的变化曲线如下图a、b所示,下列说法正确的是(______)
CH3OH(g),其两种反应过程中能量的变化曲线如下图a、b所示,下列说法正确的是(______)
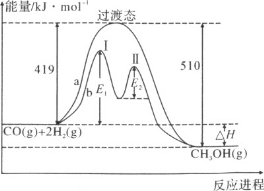
A.上述反应的ΔH=-91kJ·mol-1
B.a反应正反应的活化能为510kJ·mol-1
C.b过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
D.b过程使用催化剂后降低了反应的活化能和ΔH
E.b过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
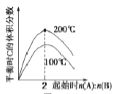
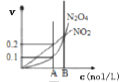
(3)①在1L的恒定密闭容器中按物质的量之比1︰2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化情况如图1所示,则压强P2________P1(填“>”、“<”或“=”);平衡由A点移至C点、D点移至B点,分别可采取的具体措施为________、________;在c点时,CO的转化率为________。
②甲和乙两个恒容密闭容器的体积相同,向甲中加入1molCO和2molH2,向乙中加入2molCO和4molH2,测得不同温度下CO的平衡转化率如图2所示,则L、M两点容器内压强:P(M)________2P(L);平衡常数:K(M)________K(L)。(填“>”、“<”或“=”)

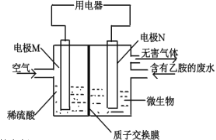
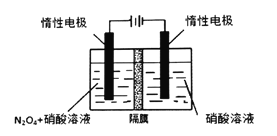
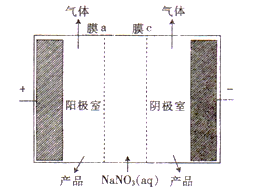
(4)以纳米二氧化钛膜为工作电极,稀硫酸为电解质溶液,在一定条件下通入CO2进行电解,在阴极可制得低密度聚乙烯![]() (简称LDPE)。
(简称LDPE)。
①电解时,阴极的电极反应式是________。
②工业上生产1.4×102kg的LDPE,理论上需要标准状况下________L的CO2。