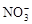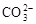题目内容
下列表述或判断正确的是( )
| A.25℃时,pH=10的NaOH溶液与pH=10的氨水中:c(Na+)=c(NH4+) |
| B.相同条件下等物质的量浓度的①NaCl 溶液;②NaOH溶液;③HCl溶液中由水电离出的c(H+):③>①>② |
| C.在Na2CO3、NaHCO3两种溶液中,离子种类不相同 |
| D.25℃时,浓度为0.2 mol·L-1的Na2CO3溶液中只存在水解平衡,不存在电离平衡 |
A
试题分析:根据电荷守恒可知,c(Na+)+c(H+)=c(OH-)、c(NH4+)+c(H+)=c(OH-)。由于溶液中氢离子浓度和c(OH-)分别都是相等的,所以c(Na+)=c(NH4+),A正确;在物质的量浓度相等的条件下,氢氧化钠和盐酸对水的抑制程度是相同,而氯化钠溶液不影响水的电离,B不正确;C不正确,离子的种类是相同的,都含有H+、OH-、CO32-、HCO3-、Na+;D不正确,还存在水的电离平衡,答案选A。
点评:该题属于中等难度的试题,关键是熟练应用所学知识解决实际问题的能力,以及对基础知识的熟练掌握程度。但该题可能会错选D,主要是做题不够灵活,没有考虑到水的电离平衡导致的。

练习册系列答案
相关题目
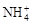 、Cu2+、
、Cu2+、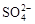 、
、