题目内容
下列离子或分子组中能大量共存且满足相应要求的是
| 选项 | 离子 | 要求 |
| A | K+、AlO、Cl-、MnO | c(K+)<c(Cl-) |
| B | Fe3+、NO、I-、HCO | 逐滴滴加盐酸立即有气体产生 |
| C | NH、Al3+、SO、CH3COOH | 滴加NaOH溶液立刻有气体产生 |
| D | Na+、Cu2+、Cl-、SO | 逐滴滴加氨水先有沉淀产生,后沉淀消失 |
D
试题分析:选项A中如果钾离子浓度小于氯离子浓度,则不能符合电荷守恒定律,A不正确;B中Fe3+和I-以及HCO3-不能大量共存;C中氢氧化钠首先和醋酸反应,开始没有气体生成,所以正确的答案选D。
点评:离子不能大量共存的一般情况是(1)能发生复分解反应的离子之间(即生成沉淀,气体,水、弱酸、弱碱等难电离物质)。(2)能生成微溶物的离子之间(如:Ca2+和 SO42-;Ag+和 SO42-)。(3)能完全水解的离子之间,如多元弱酸和弱碱盐的阴、阳离子(如:Al3+, Fe3+与 CO32-、HCO3-、AlO2-、ClO-,S2-等)。(4)能发生氧化还原反应的离子之间(如:Fe 、H+、NO3-;S2-、ClO-;S2-、 Fe3+等)。(5)能发生络合反应的离子之间(如 Fe3+和 SCN-)。解决离子共存问题时还应该注意题目所隐含的条件,题目所隐含的条件一般有(1)溶液的酸碱性,据此来判断溶液中是否有大量的 H+或 OH-。(2)溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在。(3)溶液的具体反应条件,如“氧化还原反应”“加入铝粉产生氢气” 。(4)是“可能”共存,还是“一定”共存。

练习册系列答案
相关题目

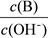 ②
②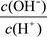 ③c(H+)
③c(H+) 下列各组离子可能大量共存的是( ):
下列各组离子可能大量共存的是( ):