题目内容
16.下列叙述中,正确的是( )| A. | 用10ml的量筒准确量取8.80ml的稀硫酸 | |
| B. | 用NaOH溶液作标准液滴定未知浓度的醋酸,选择甲基橙做指示剂 | |
| C. | 测定中和反应的热反应,将碱缓慢倒入酸中,所测温度值不变 | |
| D. | 氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中 |
分析 A.量筒精确到0.1mL;
B.滴定终点呈碱性,应用酚酞作指示剂;
C.测定中和反应的热反应,应防止热量散失;
D.氯水中次氯酸以及硝酸银见光易分解.
解答 解:A.量筒精确到0.1mL,不能量取8.80mL的稀硫酸,故A错误;
B.醋酸为弱酸,滴定终点呈碱性,应用酚酞作指示剂,故B错误;
C.测定中和反应的热反应,应防止热量散失,应将碱液迅速倒入酸中,故C错误;
D.氯水中次氯酸以及硝酸银见光易分解,应避光保存,保存在棕色玻璃瓶中,故D正确.
故选D.
点评 本题考查较为综合,涉及仪器的使用、滴定、中和热的测定以及药品的保存等问题,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质以及实验的严密性、可行性的评价,难度不大.

练习册系列答案
相关题目
6.下列物质,不属于合金的是( )
| A. | 硬铝 | B. | 青铜 | C. | 水银 | D. | 钢 |
7.化学变化中,反应物的总能量低于生成物的总能量的是( )
| A. | 2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$2H2O | |
| B. | CaO+H2O=Ca(OH)2 | |
| C. | CaCO3 $\frac{\underline{\;\;△\;\;}}{\;}$CaO+CO2↑ | |
| D. | CH3CH2OH(酒精)+3O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2+3 H2O |
4.下列说法或做法中正确的是( )
| A. | 氟氯烃的大量排放是造成酸雨的主要原因 | |
| B. | 等质量的同种煤粉和煤块完全燃烧,放出热量前者大于后者 | |
| C. | 液氯泄漏事故发生时,周边的人应该朝顺风方向逃逸或向避风的沟塘低洼处转移 | |
| D. | 火箭发动机有偏二甲肼(C2H8N2)与N2O4混合后充分燃烧,可生成CO2、N2和H2O |
1.C和CuO在一定温度下反应,产物有Cu、Cu2O、CO、CO2.将1.20g C跟16.0g CuO混合,隔绝空气加热,将生成的气体全部通过足量的澄清石灰水,反应一段时间后共收集到1.12L气体(标准状况),生成沉淀的质量为5.00g.下列说法正确的是( )
| A. | 反应后的固体混合物中还含有碳 | |
| B. | 反应后的固体混合物总质量为12.8 g | |
| C. | 反应后的固体混合物中氧化物的物质的量为0.05 mol | |
| D. | 反应后的固体混合物中单质Cu的质量为12.8 g |
8.下列依据相关实验得出的结论正确的是( )
| A. | 将某无色气体通入品红溶液中,品红溶液褪色,则此气体一定是SO2 | |
| B. | 取少许某溶液并滴加数滴硫氰化钾溶液,无明显现象,再滴加数滴H2O2溶液,溶液变血红色,则原溶液中一定含Fe2+ | |
| C. | 在硫酸钡沉淀中加入浓碳酸钠溶液充分搅拌后,取沉淀(洗净)放入盐酸中有气泡产生,说明Ksp(BaCO3)<Ksp(BaSO4) | |
| D. | 在淀粉溶液中加入稀硫酸并加热片刻再加入适量银氨溶液,水浴加热后没有银镜生成,说明淀粉没有水解 |
9.高锰酸钾[KMnO4]是常用的氧化剂,工业上以软锰矿(主要成分是MnO2)为原料制备高锰酸钾晶体.中间产物为锰酸钾[K2MnO4],如图是实验室模拟制备的操作流程:
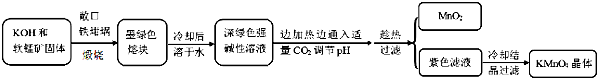
相关资料:
①物质溶解度
②锰酸钾[K2MnO4]
外观性状:墨绿色结晶.其水溶液呈深绿色,这是锰酸根(MnO42-)的特征颜色.
化学性质:在强碱性溶液中稳定,在酸性、中性和弱碱性环境下,MnO42-会发生歧化反应.
试回答下列问题:
(1)煅烧软锰矿和KOH固体时,不采用石英坩埚而选用铁坩埚的理由是瓷坩埚中的二氧化硅和强碱反应,坩埚被腐蚀;实验中用铁坩锅煅烧暴露在空气中的固体混合物发生反应的化学方程式为2MnO2+4KOH+O2$\frac{\underline{\;高温\;}}{\;}$2K2MnO4+2H2O.
(2)实验时,若CO2过量会生成KHCO3,导致得到的KMnO4产品的纯度降低.请写出实验中通入适量CO2时体系中可能发生反应离子方程式:3MnO42-+2CO2═2MnO4-+MnO2↓+2CO32-、2OH-+CO2═CO32-+H2O;
(3)由于CO2的通入量很难控制,因此对上述实验方案进行了改进,即把实验中通CO2改为加其他的酸.从理论上分析,选用下列酸中a,得到的产品纯度更高.
a.醋酸b.浓盐酸c.稀硫酸.
(4)工业上一般采用惰性电极电解锰酸钾溶液制取高锰酸钾,试写出该电解反应的化学方程式:2K2MnO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2KMnO4+H2↑+2KOH;传统工艺采用无膜电解法由于副反应发生,Mn元素利用率和电流效率都会偏低.有同学联想到离子交换膜法电解饱和食盐水提出改进方法:可用阳离子交换膜分隔两极区进行电解(如图)图中A口加入的溶液最好为KOH溶液.使用阳离子交换膜可以提高Mn元素利用率的原因为阳离子交换膜防止锰酸根进入阴极区被还原.

相关资料:
①物质溶解度
| 物质 | KMnO4 | K2CO3 | KHCO3 | K2SO4 | CH3COOK |
| 20℃溶解度 | 6.4 | 111 | 33.7 | 11.1 | 217 |
外观性状:墨绿色结晶.其水溶液呈深绿色,这是锰酸根(MnO42-)的特征颜色.
化学性质:在强碱性溶液中稳定,在酸性、中性和弱碱性环境下,MnO42-会发生歧化反应.
试回答下列问题:
(1)煅烧软锰矿和KOH固体时,不采用石英坩埚而选用铁坩埚的理由是瓷坩埚中的二氧化硅和强碱反应,坩埚被腐蚀;实验中用铁坩锅煅烧暴露在空气中的固体混合物发生反应的化学方程式为2MnO2+4KOH+O2$\frac{\underline{\;高温\;}}{\;}$2K2MnO4+2H2O.
(2)实验时,若CO2过量会生成KHCO3,导致得到的KMnO4产品的纯度降低.请写出实验中通入适量CO2时体系中可能发生反应离子方程式:3MnO42-+2CO2═2MnO4-+MnO2↓+2CO32-、2OH-+CO2═CO32-+H2O;

(3)由于CO2的通入量很难控制,因此对上述实验方案进行了改进,即把实验中通CO2改为加其他的酸.从理论上分析,选用下列酸中a,得到的产品纯度更高.
a.醋酸b.浓盐酸c.稀硫酸.
(4)工业上一般采用惰性电极电解锰酸钾溶液制取高锰酸钾,试写出该电解反应的化学方程式:2K2MnO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2KMnO4+H2↑+2KOH;传统工艺采用无膜电解法由于副反应发生,Mn元素利用率和电流效率都会偏低.有同学联想到离子交换膜法电解饱和食盐水提出改进方法:可用阳离子交换膜分隔两极区进行电解(如图)图中A口加入的溶液最好为KOH溶液.使用阳离子交换膜可以提高Mn元素利用率的原因为阳离子交换膜防止锰酸根进入阴极区被还原.
10.如图是元素周期表的一部分,下列说法正确的是( )
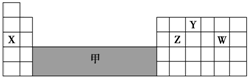

| A. | 可在灰色区域“甲”中寻找半导体材料 | |
| B. | X、Z、W 最高价氧化物对应的水化物之间两两能相互反应 | |
| C. | 气态氢化物的稳定性:Z<W | |
| D. | X只能形成一种氧化物 |
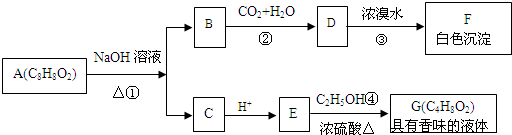
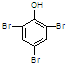 ;
; ;
; .
.