题目内容
4.下列叙述正确的是(NA为阿伏加德罗常数的数值)( )| A. | 22.4LCO2含有NA个CO2分子 | B. | 0.1NA个H2SO4分子的质量为9.8克 | ||
| C. | 10gCaCO3含有NA个C原子 | D. | 2molCl2含有2NA个Cl原子 |
分析 A.气体状况未知;
B.依据m=$\frac{N}{{N}_{A}}$×M计算;
C.质量转化为物质的量,结合1mol碳酸钙含有1mol碳原子;
D.1个氯气分子含有2个氯原子.
解答 解:A.气体状况未知,无法计算二氧化碳物质的量,故A错误;
B.0.1NA个H2SO4分子的质量为$\frac{0.1{N}_{A}}{{N}_{A}}$×98g/mol=9.8g,故B正确;
C.10gCaCO3物质的量为$\frac{10g}{100g/mol'}$=0.1mol,含有0.1NA个C原子,故C错误;
D.2molCl2含有4NA个Cl原子,故D错误;
故选:B.
点评 本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系是解题关键,注意气体摩尔体积使用条件和对象,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.已知反应:
①2C(s)+O2(g)═2CO(g)△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol
下列结论正确的是( )
①2C(s)+O2(g)═2CO(g)△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol
下列结论正确的是( )
| A. | 碳的燃烧热110.5 kJ/mol | |
| B. | ①的反应热为221 kJ/mol | |
| C. | 稀醋酸与稀NaOH溶液反应的中和热为57.3kJ/mol | |
| D. | 稀盐酸与稀NaOH溶液反应的中和热为57.3kJ/mol |
9.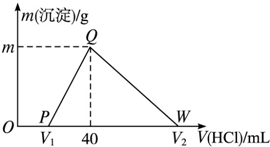 常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol•L-1的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是( )
常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol•L-1的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是( )
 常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol•L-1的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是( )
常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol•L-1的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是( )| A. | 原合金质量为0.92g | B. | 图中V2为60 | ||
| C. | 沉淀的质量m为1.56g | D. | OP段发生的反应为:OH-+H+═H2O |
16.在一定条件下化学反应:2SO2(g)+O2(g)═2SO3(g)△H=-197kJ/mol 现有容积相同且固定不变的甲、乙、丙三个容器,在上述条件下分别充入的气体和反应放出的热量(Q)如下表所列:
根据以上数据,下列叙述不正确的是( )
| 容器 | SO2(mol) | O2(mol) | N2(mol) | Q(kJ) |
| 甲 | 2 | 1 | 0 | Q1 |
| 乙 | 1 | 0.5 | 0 | Q2 |
| 丙 | 1 | 0.5 | 1 | Q3 |
| A. | Q2=Q3<98.5kJ | |
| B. | Q1=2Q2=2Q3=197kJ | |
| C. | 2Q2=2Q3<Q1<197kJ | |
| D. | 在上述条件下反应生成1molSO3气体放热98.5kJ |
13.我国规定食盐的含碘量(按每千克食盐含碘元素计)为20~40mg/Kg,则每千克食盐中加入碘酸钾的物质的量应不少于(设碘酸钾的摩尔质量为M g/mol)( )
| A. | $\frac{20×1{0}^{-3}}{127}$mol | B. | 20M mol | C. | $\frac{20×1{0}^{-3}}{M}$mol | D. | $\frac{20}{M}$mol |
6.Ⅰ.(1)已知某有机物A只含有C、H、O三种元素,通过元素分析知含碳54.55%,含氢9.10%.质谱分析其相对分子质量为88,经红外光谱分析其中只含C-H键和 键,其核磁共振氢谱图显示有三重峰,峰面积之比为3:2:3,该有机物不含有CH3-O-,则A的结构简式为CH3COOCH2CH3.
键,其核磁共振氢谱图显示有三重峰,峰面积之比为3:2:3,该有机物不含有CH3-O-,则A的结构简式为CH3COOCH2CH3.
(2)写出实验室制备A的化学方程式CH3COOH+HOCH2CH3$\stackrel{浓硫酸}{?}$CH3COOCH2CH3+H2O.
Ⅱ.苯甲酸甲酯 是常用香精,广泛用于食品、化妆品等行业,可从自然界中提取,也可人工合成.实验室现以食品防腐剂[主要成分为苯甲酸钠(
是常用香精,广泛用于食品、化妆品等行业,可从自然界中提取,也可人工合成.实验室现以食品防腐剂[主要成分为苯甲酸钠(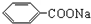 )]、甲醇为原料制备苯甲酸甲酯.已知:
)]、甲醇为原料制备苯甲酸甲酯.已知:
合成苯甲酸甲酯的流程如下:

请回答下列问题:
(1)温度①约为64.7℃,操作③为分液,操作④为蒸馏.
(2)第②步加热的目的是蒸出过量的甲醇.
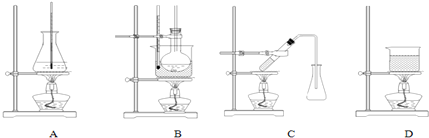
(3)选择合适的制备苯甲酸甲酯的装置:B.
(4)苯甲酸甲酯有多种同分异构体,写出符合下列条件的任意一种同分异构体的结构简式 .
.
①为芳香化合物 ②含有醛基 ③能与金属Na反应.
 键,其核磁共振氢谱图显示有三重峰,峰面积之比为3:2:3,该有机物不含有CH3-O-,则A的结构简式为CH3COOCH2CH3.
键,其核磁共振氢谱图显示有三重峰,峰面积之比为3:2:3,该有机物不含有CH3-O-,则A的结构简式为CH3COOCH2CH3.(2)写出实验室制备A的化学方程式CH3COOH+HOCH2CH3$\stackrel{浓硫酸}{?}$CH3COOCH2CH3+H2O.
Ⅱ.苯甲酸甲酯
 是常用香精,广泛用于食品、化妆品等行业,可从自然界中提取,也可人工合成.实验室现以食品防腐剂[主要成分为苯甲酸钠(
是常用香精,广泛用于食品、化妆品等行业,可从自然界中提取,也可人工合成.实验室现以食品防腐剂[主要成分为苯甲酸钠( )]、甲醇为原料制备苯甲酸甲酯.已知:
)]、甲醇为原料制备苯甲酸甲酯.已知:| 熔点℃ | 沸点℃ | 水溶性 | |
| 甲醇 | -97.8 | 64.7 | 易溶 |
| 苯甲酸 (一元弱酸) | 122.4 | 249.3 | 常温:0.17g 100℃:6.8g |
| 苯甲酸甲酯 | -12.3 | 198 | 难溶 |

请回答下列问题:
(1)温度①约为64.7℃,操作③为分液,操作④为蒸馏.
(2)第②步加热的目的是蒸出过量的甲醇.
(3)选择合适的制备苯甲酸甲酯的装置:B.

(4)苯甲酸甲酯有多种同分异构体,写出符合下列条件的任意一种同分异构体的结构简式
 .
.①为芳香化合物 ②含有醛基 ③能与金属Na反应.
 烯烃A在一定条件下可以按如图的框图进行反应.
烯烃A在一定条件下可以按如图的框图进行反应.