题目内容
12.用来表示可逆反应:A(g)+B(g)?2C(g)(正反应放热)的正确图象是如图中的( )| A. | 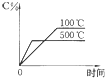 | B. |  | C. | 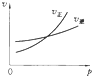 | D. | 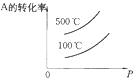 |
分析 根据方程式可知,正反应放热,则升高温度正逆反应速率都增大,平衡向逆反应方向移动,C的含量降低,A的转化率降低,由于反应前后气体的体积不变,则增大压强平衡不移动,正逆反应速率增大的倍数相同.
解答 解:A.正反应放热,则升高温度正逆反应速率都增大,平衡向逆反应方向移动,C的含量降低,图象吻合,故A正确;
B.升高温度正逆反应速率都增大,图象不吻合,故B错误;
C.由于反应前后气体的体积不变,则增大压强平衡不移动,正逆反应速率增大的倍数相同,图象不吻合,故C错误;
D.由于反应前后气体的体积不变,则增大压强平衡不移动,则A的转化率不变,故D错误.
故选A.
点评 本题考查化学平衡图象问题,题目难度中等,解答本题的关键是根据反应的特征判断外界条件对平衡移动的影响,与图象对比可解答该题.

练习册系列答案
相关题目
2.下述实验操作与预期实验目的或所得实验结论不一致的是( )
| 编号 | 实验操作 | 实验目的或结论 |
| A | 将SO2气体通入紫色石蕊试液中,观察溶液是否褪色 | 证明SO2有漂白性 |
| B | 向试管中加入等体积的0.005mol/L的FeCl3溶液和0.01mol/L的KSCN溶液,再滴加几滴饱和FeCl3溶液,观察颜色变化 | 探究增大反应物浓度时平衡移动的方向 |
| C | 将装有NO2和N2O4气体的联通球,一个置于冰水中,一个置于热水中,观察颜色变化 | 探究温度对化学平衡的影响 |
| D | 将CO2通入Na2SiO3水溶液观察是否有沉淀产生 | 探究碳和硅两元素非金属性强弱 |
| A. | A | B. | B | C. | C | D. | D |
3.在一定体积的密闭容器中,进行如下化学反应:
CO(g)+H2O(g)$\frac{\underline{\;催化剂\;}}{\;}$CO2(g)+H2(g),其化学平衡常数K和温度t的关系如表:
请回答下列问题:
(1)该反应的化学平衡常数表达式为K=$\frac{C(CO{\;}_{2})•C(H{\;}_{2})}{C(CO)•C(H{\;}_{2}O)}$,该反应为放热反应(填“吸热”或
“放热”).
(2)能判断该反应是否达到化学平衡状态的依据是BC.
A.容器中压强不变
B.混合气体中c(CO)不变
C.v生成(H2)=v消耗(H2)
D.c(CO2)=c(CO)
(3)830℃时,容器中的反应已达到平衡.在其他条件不变的情况下,缩小容器的体积,平衡不移动(填“向正反应方向”、“向逆反应方向”或“不”).
CO(g)+H2O(g)$\frac{\underline{\;催化剂\;}}{\;}$CO2(g)+H2(g),其化学平衡常数K和温度t的关系如表:
| t/(℃) | 700 | 80 | 830 | 1000 | 1200 |
| K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的化学平衡常数表达式为K=$\frac{C(CO{\;}_{2})•C(H{\;}_{2})}{C(CO)•C(H{\;}_{2}O)}$,该反应为放热反应(填“吸热”或
“放热”).
(2)能判断该反应是否达到化学平衡状态的依据是BC.
A.容器中压强不变
B.混合气体中c(CO)不变
C.v生成(H2)=v消耗(H2)
D.c(CO2)=c(CO)
(3)830℃时,容器中的反应已达到平衡.在其他条件不变的情况下,缩小容器的体积,平衡不移动(填“向正反应方向”、“向逆反应方向”或“不”).
20.晶胞是晶体结构中可重复出现的最小的结构单元,C60晶胞结构如图所示,下列说法正确的是( )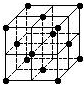

| A. | C60摩尔质量是720 | |
| B. | C60属于离子晶体 | |
| C. | 在C60晶胞中有14个C60分子 | |
| D. | 每个C60分子周围与它距离最近等距离的C60分子有12个 |
7.下列操作达不到预期目的是( )
①将某卤代烃与氢氧化钠的水溶液共热,向冷却后的反应液中滴加AgNO3溶液,若产生白色沉淀,则证明该卤代烃为氯代烃
②用乙醇和30%的硫酸共热到170℃制取乙烯
③在苯酚中滴入少量溴水出现白色沉淀
④将苯与浓硝酸混合加热至60℃制备硝基苯
⑤检验淀粉已经水解,将淀粉与少量稀硫酸加热一段时间后,再加入银氨溶液加热.
①将某卤代烃与氢氧化钠的水溶液共热,向冷却后的反应液中滴加AgNO3溶液,若产生白色沉淀,则证明该卤代烃为氯代烃
②用乙醇和30%的硫酸共热到170℃制取乙烯
③在苯酚中滴入少量溴水出现白色沉淀
④将苯与浓硝酸混合加热至60℃制备硝基苯
⑤检验淀粉已经水解,将淀粉与少量稀硫酸加热一段时间后,再加入银氨溶液加热.
| A. | ①③④ | B. | ②③⑤ | C. | ①②④⑤ | D. | ①②③④⑤ |
17.下列叙述正确的是( )
| A. | 1molH2O的质量为18g/mol | |
| B. | O2 的摩尔质量为32g | |
| C. | 2mol NaOH 溶于1 L水中配成溶液的浓度为2mol/L | |
| D. | 6.02×1023个CO分子的质量约为28g |
4.根据下列反应:①H2S+I2═S↓+2HI;②2FeCl3+2HI═2FeCl2+2HCl+I2;③2FeCl2+Cl2═2FeCl3,可以判断有关物质的氧化性由强到弱的顺序正确的是( )
| A. | Cl2>Fe3+>I2>S | B. | S>I2>Fe3+>Cl2 | C. | Fe3+>Cl2>H2S>I2 | D. | Cl2>I2>Fe3+>H2S |
1.下列物质发生变化时,所克服的粒子间相互作用属同种类型的是( )
| A. | 碘与干冰分别受热变为气体 | B. | 硝酸铵与硝酸分别受热变为气体 | ||
| C. | 氯化钠与氯化氢分别溶解在水中 | D. | 氧化铝与冰分别受热熔化 |
2.已知有机物X、Y均具有CH2的最简式,则下列说法中不正确的是( )
| A. | 将X、Y完全燃烧后生成CO2和H2O的物质的量之比均为1:1 | |
| B. | 将等质量的X、Y完全燃烧时消耗O2的量一定相等 | |
| C. | 将等物质的量的X、Y完全燃烧时消耗O2的量一定相等 | |
| D. | 无论X、Y以何种比例混合,只要总质量一定,完全燃烧时消耗的O2的量一定相等 |