��Ŀ����
����Ŀ�����ǻ��õļ����Ԫ�أ��Ƽ��仯�������������������й㷺��Ӧ�á�
��1����������(NaN3)��ײ����ȫ�ֽ�����ƺ͵������ʿ�Ӧ����������ȫ���ҡ������� 6.72 L(��״����)������������Ҫ��������_____g��
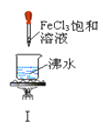
��2��Ϊʵ�ֽ������ڸ���������������ˮ��Ӧ���ռ����ɵ����壬ij�о� ��ѧϰС���������ͼ����װ�ã�
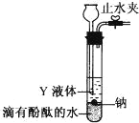
��д�� Na ��ˮ��Ӧ�����ӷ���ʽ_____��
��Y Һ�����ѡ��_____
A��ú�� B���ƾ� C�����Ȼ�̼
��ʵ��ǰ�����װ�������Եķ����ǣ��ر�ֹˮ�У�ͨ��_________����װ�����ƣ����Թ��м�ˮ������Һ��һ��ʱ���_____�������������������á�
��3��1mol ���������� 1.6mol ̼�����ƹ����Ϻ����ܱյ������м��ȳ�ַ�Ӧ���ų��������ʺ���ȴ�������Ĺ������ʼ���Ӧ�����ʵ���(�ɲ�����)��
���� | ���ʵ���/mol |
__________ | __________ |
__________ | __________ |
���𰸡�13 g 2Na+2H2O=2Na++2OH-+H2 A ����©�� Һ���� Na2CO3 1.6 NaOH 0.4
��������
(1)������Ӧ��2NaN3=2Na+3N2�������ݷ���ʽ���㣻
(2)�� Na ��ˮ��Ӧ����NaOH��������
�ڸ���װ�ÿ�֪YҺ���ܶ�С��ˮ������ˮ���ܣ�
������Һѹ��ȷ��װ�������ԣ�
(3)���ȷ���2NaHCO3![]() Na2CO3+CO2��+H2O��Ȼ����2Na2O2+2CO2�T2Na2CO3+O2��2Na2O2+2H2O�T4NaOH+O2�����Դ������
Na2CO3+CO2��+H2O��Ȼ����2Na2O2+2CO2�T2Na2CO3+O2��2Na2O2+2H2O�T4NaOH+O2�����Դ������
(1)����ҪNaN3 ������Ϊm����
2NaN3![]() 2Na+3N2��
2Na+3N2��
130g 67.2L
m 6.72L
m=![]() =13g��
=13g��
(2)�� Na ��ˮ��Ӧ����NaOH�����������ӷ���ʽΪ2Na+2H2O=2Na++2OH-+H2����
��װ�ÿ�֪YҺ���ܶ�С��ˮ������ˮ���ܣ�
A��ú���ܶ�С��ˮ������ˮ���ܣ���A��ȷ��
B���ƾ���ˮ���ܣ���B����
C�����Ȼ�̼�ܶȴ���ˮ������ˮ���ܣ���C����
�ʴ�ΪA��
��ʵ��ǰ�����װ�������Եķ����ǣ��ر�ֹˮ�У���©����עˮ��ֱ������©���е�Һ������Թ��е�Һ�棬������Һ���ٸı䣬��֤����װ�����������ã�
(3)��2NaHCO3![]() Na2CO3+CO2��+H2O��֪��1.6mol̼�����Ʒֽ�����0.8molNa2CO3��0.8molCO2��0.8molH2O����2Na2O2+2CO2�T2Na2CO3+O2��֪��0.8molCO2��0.8molNa2O2��Ӧ����0.8molNa2CO3��2Na2O2+2H2O�T4NaOH+O2����0.2molNa2O2��ˮ��Ӧ����0.4molNaOH����ַ�Ӧ���ų��������ʺ���ȴ��������Ĺ���������NaOH��Na2CO3�����ߵ����ʵ����ֱ�Ϊ0.4mol��1.6mol��
Na2CO3+CO2��+H2O��֪��1.6mol̼�����Ʒֽ�����0.8molNa2CO3��0.8molCO2��0.8molH2O����2Na2O2+2CO2�T2Na2CO3+O2��֪��0.8molCO2��0.8molNa2O2��Ӧ����0.8molNa2CO3��2Na2O2+2H2O�T4NaOH+O2����0.2molNa2O2��ˮ��Ӧ����0.4molNaOH����ַ�Ӧ���ų��������ʺ���ȴ��������Ĺ���������NaOH��Na2CO3�����ߵ����ʵ����ֱ�Ϊ0.4mol��1.6mol��

 ������״Ԫ��ҵϵ�д�
������״Ԫ��ҵϵ�д� ��ʱ�ƿ�������ϰϵ�д�
��ʱ�ƿ�������ϰϵ�д� һ��һ��һ��ͨϵ�д�
һ��һ��һ��ͨϵ�д�����Ŀ�����û�ѧԭ�����ԶԹ����ŷŵķ�ˮ�������Ƚ�����Ч��������������ij�������Ƹ﹤ҵ������Cr(III)�Ĵ���������������:

��֪:�������ȡҺ�еĽ���������Ҫ��Cr3+�������Fe2+��Al3+��Ca2+��Mg2+����Cr2O72-+H2O![]() 2CrO42-+2H+���۳����£�����������������������ʽ����ʱ��Һ��pH����:
2CrO42-+2H+���۳����£�����������������������ʽ����ʱ��Һ��pH����:
������ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
������ȫʱ��pH | 3.2 | 11.1 | 5.4(>8�ܽ�) | 9(>9�ܽ�) |
(1) ʵ������18.4mol/L��Ũ��������480mL2mol/L�����ᣬ����ȡŨ����_____mL������ʱ����Ͳ���ձ��Ͳ������⣬�����õ��IJ���������______________��
(2) H2O2�������ǽ���ҺI�е�Cr3+ת��ΪCr2O72-,д���˷�Ӧ�����ӷ���ʽ:__________��
(3����II�����õ���������ҪΪ______(�ѧʽ),��ҺII�к��е�������Ҫ��__��
(4) �����ӽ�����֬�ķ�Ӧԭ��Ϊ:Mn++nNaR=MRn+nNa+,�����������ӽ�����֬�ɳ�ȥ��ҺII�еĽ�����������_______________��
(5) д��������������SO2���л�ԭʱ������Ӧ�����ӷ���ʽ__________��
����Ŀ���±����й�������;�����ʵ���������ȷ�����������ϵ���ǣ� ��
ѡ�� | ��; | ���� |
A | �ƼغϽ�����ԭ�ӷ�Ӧ�ѵĵ��ȼ� | �ƻ�ѧ���ʺܻ��� |
B | KI�����������ӵ��� | I�����л�ԭ�ԣ��ױ�����ΪI2 |
C | 84����Һ���ڻ������� | NaClO��H2O��CO2��Ӧ����HClO |
D | Na2CO3����ʳƷ���ɼ� | Na2CO3�����ܲ������� |
A.AB.BC.CD.D