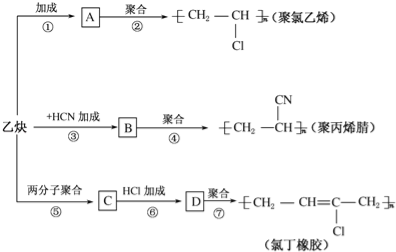
题目内容
【题目】(1)海水中蕴含的元素有80多种,它是一个巨大的宝藏。
①海水中被称为海洋元素是___。(填元素名称)
②下列物质不经过化学变化就能从海水中获得的是___。(填字母)
A.单质钠 B.单质碘 C.氯化钠
③加碘食盐中碘酸钾的化学式是___。
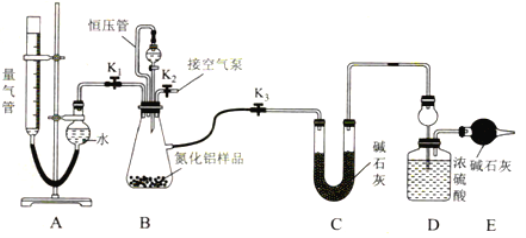
(2)实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
①在该反应的化学方程式上用双线桥标出电子转移的方向和数目___。
②该反应中浓盐酸表现的性质有___。
③如反应中转移了20mol电子,则产生的Cl2在标准状况下体积为__ L。
【答案】溴 C KIO3 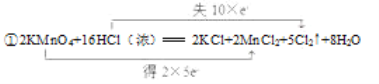 还原性和酸性 224
还原性和酸性 224
【解析】
(1)①海洋元素是溴的一个别名,因为99%的溴都在海洋里;
答案是溴;
②海水中含有氯化钠,通过蒸发结晶就可以得到,钠和碘都以化合态的形式存在海水中,需要得到单质,需要通过化学反应;
答案是C;
③碘酸钾的化学式为KIO3;
答案是KIO3;
(2) ① 2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,KMnO4中的Mn的化合价从+7价降低到+2价,则2molKMnO4共得到10mol电子;HCl中的Cl的化合价从-1升高到0,总有10molHCl中的Cl化合价升高,共得到10mol电子,双线桥,箭头从反应物中化合价发生变化的元素指向生成物中化合价发生变化的元素,并在写上转移的电子数目;
答案为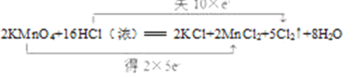 ;
;
②在该反应中,HCl中部分Cl的化合价从-1升高到O,表现出还原性,有部分Cl的化合价没有变化,得到KCl和MnCl2,表现出酸性;
答案是还原性和酸性;
③化学方程式中,转移10mol电子,得到5molCl2,转移20mol电子,则得到10molCl2,则产生的Cl2在标准状况下体积为10×22.4L=224L;
答案为224。

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案【题目】下列实验所用试剂、现象和结论均正确的是
选项 | 实验装置 | 现象 | 结论 |
A |
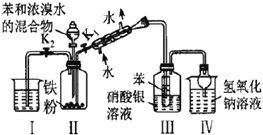
| 装置Ⅲ中有浅黄色沉淀 | 苯和浓溴水发生取代反应 |
B |
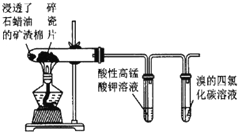
| 高锰酸钾溶液褪色,溴的四氯化碳溶液褪色 | 石蜡油的分解产物中含有不饱和烃 |
C |
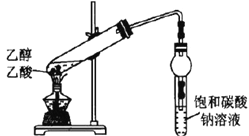
| 盛有饱和碳酸钠溶液的试管中,上方出现油状液体 | 制备乙酸乙酯 |
D |
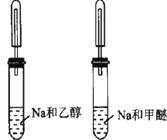
| 甲醚有气泡 | 鉴别乙醇与甲醚(CH3OCH3) |
A. A B. B C. C D. D