题目内容
14.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )| A. | 10g重水(2H216O)中含有的中子数目为5NA | |
| B. | 28g氮气所含有的原子数目为NA | |
| C. | 标准状况下,2.24L水中含有的水分子数目为0.1NA | |
| D. | 1mol铁与足量稀盐酸反应转移的电子数目为3NA |
分析 A、求出重水的物质的量,然后根据1mol重水中含10mol中子来计算;
B、根据氮气由氮原子构成来分析;
C、标况下,水为液态;
D、铁与盐酸反应后变为+2价.
解答 解:A、重水的摩尔质量为20g/mol,故10g重水的物质的量为0.5mol,而1mol重水中含10mol中子,故0.5mol重水中含5mol中子即5NA个,故A正确;
B、氮气由氮原子构成的,故28g氮气中含有的氮原子的物质的量n=$\frac{28g}{14g/mol}$=2mol,个数为2NA个,故B错误;
C、标况下,水为液态,不能根据气体摩尔体积来计算其物质的量,故C错误;
D、铁与盐酸反应后变为+2价,故1mol铁转移2mol电子即2NA个,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
8.下列指定反应的离子方程式正确的是( )
| A. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液至SO42-恰好沉淀完全:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O | |
| B. | 将标准状况下1.12L氯气通入10mL 1mol•L-1的溴化亚铁溶液中:2Fe2++2Br-+2Cl2=2Fe3++4Cl-+Br2 | |
| C. | 氢氧化铁溶于氢碘酸溶液:2Fe(OH)3+6H++2I-═2Fe2++I2+6H2O | |
| D. | 4mol•L-1的NaAlO2溶液和7mol•L-1的盐酸等体积混合:AlO2-+4H+=Al3++2H2O |
4.在4℃时,100mL水中溶解了22.4L HCl气体(标准状况)后形成盐酸溶液.下列关于该溶液的说法中正确的是( )
| A. | 该溶液物质的量浓度为10mol•L-1 | |
| B. | 该溶液物质的量浓度因溶液的密度未知而无法求得 | |
| C. | 所得溶液的体积为22.5L | |
| D. | 按所给条件该溶液中溶质的质量分数无法求得 |
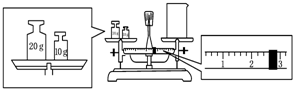 实验室欲用NaOH固体配制1.0mol•L-1的NaOH溶液250mL:
实验室欲用NaOH固体配制1.0mol•L-1的NaOH溶液250mL: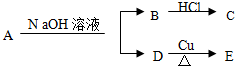 ,又已知D不与Na2CO3溶液反应,C和E都不能发生银镜反应.A的结构可能有( )
,又已知D不与Na2CO3溶液反应,C和E都不能发生银镜反应.A的结构可能有( ) 氢氧燃料电池已用于航天飞机.以30% KOH溶液为电解质溶液的这种电池的构造如图所示.该电池在工作时的电极反应如下:
氢氧燃料电池已用于航天飞机.以30% KOH溶液为电解质溶液的这种电池的构造如图所示.该电池在工作时的电极反应如下: