题目内容
【题目】下列有关电化学原理的说法错误的是( )
A.氯化铝的熔点比氧化铝低,因此工业上最好采用电解熔融氯化铝来制备单质铝
B.电镀时,通常把待镀的金属制品作阴极,把镀层金属作阳极
C.对于冶炼像钠、钙、镁、铝等这样活泼的金属,电解法几乎是唯一可行的工业方法
D.对大型船舶的外壳进行的“牺牲阳极的阴极保护法”,是应用了原电池原理
【答案】A
【解析】
试题氯化铝属于共价化合物,在熔融的状态下不能电离出阴阳离子,不具有导电性,因此用电解法制备金属铝时不能用电解熔融氯化铝的方法来制备

 名校课堂系列答案
名校课堂系列答案【题目】I.经测定乙醇的化学式是C2H6O,由于有机物普遍存在同分异构现象,推测乙醇的结构可能是下列两种之一。

为测定其结构,应利用物质的特殊性进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,请甲、乙、丙、丁4位同学利用如下图的装置进行实验,确定乙醇的结构。

(1)同学甲得到一组实验数据如表:
乙醇的物质的量/mol | 氢气的体积/L |
0.10 | 1.12(标准状况) |
根据以上数据推断乙醇的结构为______(用Ⅰ、Ⅱ表示),理由为____________;
(2)同学乙分别准确称量4.60 g乙醇进行多次实验,结果发现以排在量筒内水的体积作为生成的H2体积,换算成标准状况后都小于1.12 L。如果忽略量筒本身及乙同学读数造成的误差,乙同学认为可能是由于样品中含有少量水造成的,你认为正确吗?______(填“正确”或“不正确”)。请说明理由__________________________________________________________________。
(3)同学丙认为实验成功的关键有:①装置气密性要良好;②实验开始前准确确定乙醇的量;③钠足量;④广口瓶内水必须充满;⑤氢气体积的测算方法正确、数据准确。其中,正确的有_________________(填序号)。
(4)同学丁不想通过称量乙醇的质量来确定乙醇的量,那么还需要知道的数据是________。
(5)实验后,4名同学从乙醇的可能结构分析入手,对乙醇和钠的量的关系进行了讨论,如果乙醇的物质的量为n mol,那么对钠的物质的量的取值要求,必须是____________。
II.已知A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。

请回答下列问题:
(1)A的结构简式为______________________,在农业上可以用于________________。
(2)E的结构简式为___________________;B、D分子与金属钠反应的化学方程式为____________________________、____________________________。
【题目】某实验小组用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液进行中和热的测定。
Ⅰ.配制0.50 mol/L NaOH溶液
若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体_____g。
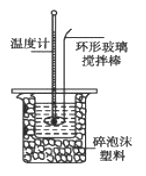
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
(1)写出该反应的热化学方程式(中和热为57.3 kJ/mol):_____________。
(2)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。
①请填写下表中的空白:
起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | |||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ______ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | ||
②近似认为0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃)。则中和热△H=______________取小数点后一位)。
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是:______。
A.实验装置保温、隔热效果差
B.量取NaOH溶液的体积时仰视读数
C.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
D.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
【题目】不同元素的原子在分子内吸引电子的能力大小可用一定数值 x 来表示,若 x 越大,其原子吸引电子能力越强,在所形成的分子中成为带负电荷的一方。
下面是某些短周期元素的 x 值:
元素符号 | Li | Be | B | C | N | F |
x 值 | 0.98 | 1.57 | 2.04 | 2.25 | 2.89 | 3.98 |
元素符号 | Na | Mg | Si | P | S | Cl |
x 值 | 0.93 | 1.35 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)通过分析 x 值变化规律,确定Al、N的 x 值范围:________< x (Al)<________
(2)推测 x 值与原子半径关系是________,根据短周期元素的 x 值变化特点,体现了元素性质的________变化规律。
(3)某有机化合物结构式为: ,其中SO键中你认为共用电子对偏向谁?________(写原子名称)。
,其中SO键中你认为共用电子对偏向谁?________(写原子名称)。
(4)经验规律告诉我们:当成键的两原子相应元素的 x 差值(Δ x )即 x >1.7时,一般为离子键;当Δ x <1.7时,一般为共价键。试推断AlF 3 中化学键类型是________。
(5)预测元素周期表中, x 值最小的元素的位置:_______(放射性元素除外)。