题目内容
11.在元素周期表中前18号元素中,其原子的最外层电子数是最内层电子数2k倍的(k为正整数)共有( )| A. | 2种 | B. | 4种 | C. | 6种 | D. | 8种 |
分析 当K=1时,则原子的最外层电子数是最内层电子数2倍有2,4;2,8,4;
当K=2时,则原子的最外层电子数是最内层电子数4倍有2,8;2,8,8;
当K=3以上都不存在,据此分析.
解答 解:当K=1时,则原子的最外层电子数是最内层电子数2倍有2,4即C;2,8,4即Si;
当K=2时,则原子的最外层电子数是最内层电子数4倍有2,8即Ne;2,8,8即Ar;
当K=3以上都不存在,所以共有4种,
故选:B.
点评 本题考查原子核外电子的分层排布规律的应用,以“周期表中前18号元素的推断”为载体,考查学生对前18号元素核外电子分层排布的掌握程度,难度不大.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
12.下列说法不正确的是( )
| A. | 标准状况下,11.2LCO2的质量为22g | |
| B. | 0.1molCl2与足量水反应转移电子0.2mol | |
| C. | 18gH2O含有的原子总数为3×6.02×1023 | |
| D. | 0.5mol/L Na2SO3溶液中Na+的物质的量浓度为1.0 mol/L |
2.下列有机物的命名正确的是( )
| A. |  2-乙基丙烷 | B. | 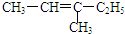 3-甲基-3-戊烯 | C. | 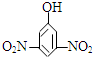 2,4-二硝基苯酚 | D. | 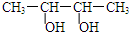 2,3-丁二醇 |
6.下列有机物的系统命名正确的是( )
| A. | 1,4-二甲基丁烷 | B. | 3,3-二甲基丁烷 | ||
| C. | 2-乙基戊烷 | D. | 4-甲基-3-乙基辛烷 |
16.一种新型燃料电池,以镍板为电极插入KOH溶液中,分别向两极通乙烷和氧气,电极反应式为:C2H6+18OH--14e-═2CO32-+12H2O;7H2O+72O2+14e-═14OH-. 有关此电池的推断错误的是( )
| A. | 此燃料电池工作时,电解质溶液中的OH-向负极移动 | |
| B. | .参加反应的O2与C2H6的物质的量之比为7:2 | |
| C. | .电池工作一段时间后,KOH的物质的量浓度将下降 | |
| D. | .通氧气的电极为负极 |
3.下列各对物质中属于同分异构体的是( )
| A. | O2与O3 | B. | CH3CH2OH与CH3CH2-O-CH2CH3 | ||
| C. | 126C与136C | D. | CH3CH2CH2CH3与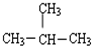 |
20.镀锌自来水管与下列水龙头连接,连接处自来水管锈蚀最快的是( )
| A. | 铜制水龙头 | B. | 铁制水龙头 | C. | 塑料水龙头 | D. | 陶瓷水龙头 |
1.符合题目要求并且正确的离子方程式的是( )
| A. | 氢氧化钡溶液与硫酸镁溶液反应:Ba2++SO42-═BaSO4↓ | |
| B. | 澄清石灰水与少量苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | 硫酸铝溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 铁屑与足量稀硝酸反应:Fe+2H+═Fe2++H2↑ |