题目内容
取8g某有机物A(相对分子质量为32)在氧气中完全燃烧,生成物中只有11g CO2和9g H2O,则A中一定含有 元素,其分子式是 ;误服A会使人中毒失明甚至死亡,其化学名称为 ,写出此物质在空气中燃烧的化学方程式 .
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:根据元素守恒可知,有机物一定含有C、H元素,根据n=
计算有机物A、CO2、H2O的物质的量,根据质量守恒判断是否含有O元素,根据原子守恒计算有机物分子中含有各元素原子数目,确定有机物A的分子式,据此解答.
| m |
| M |
解答:
解:取8g某有机物A(相对分子质量为32)在氧气中完全燃烧,生成物中只有11g CO2和9g H2O,根据元素守恒可知,有机物一定含有C、H元素,
CO2的物质的量=
=0.25mol,H2O的物质的量=
=0.5mol,故m(C)+m(H)=0.25mol×12g/mol+0.5mol×2×1g/mol=4g<8g,故有机物A还含有O元素,m(O)=8g-4g=4g,则n(O)=
=0.25mol,
8g有机物A的物质的量=
=0.25mol,有机物A中C原子数目=
=1、H原子数目=
4、O原子数目=
=1,故有机物的分子式为CH4O,结构简式为CH3OH,名称为甲醇,在空气中燃烧的化学方程式为:2CH3OH+3O2
2CO2+4H2O,
故答案为:C、H、O;CH4O;甲醇;2CH3OH+3O2
2CO2+4H2O.
CO2的物质的量=
| 11g |
| 44g/mol |
| 9g |
| 18g/mol |
| 4g |
| 16g/mol |
8g有机物A的物质的量=
| 8g |
| 32g/mol |
| 0.25mol |
| 0.25mol |
| 0.5mol×2 |
| 0.25mol |
| 0.25mol |
| 0.25mol |
| 点燃 |
故答案为:C、H、O;CH4O;甲醇;2CH3OH+3O2
| 点燃 |
点评:本题考查有机物分子式的确定,难度不大,注意利用质量守恒确定有机物中是否含有氧元素.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列离子方程式正确的是( )
| A、将过量NaOH溶液滴入Ca(HCO3)2溶液中:Ca2++HCO3-+OH-→CaCO3↓+H2O |
| B、Fe(OH)3溶于氢碘酸:2Fe(OH)3+6H++2I-→2Fe2++I2+6H2O |
| C、向硫酸铝铵[NH4Al(SO4)2]溶液中加入氢氧化钡溶液至SO42-离子沉淀完全Al3++2SO42-+2Ba2++4OH-→AlO2-+2BaSO4↓+2H2O |
| D、4mol?L-1的NaAlO2溶液和7mol?L-1的HCl等体积互相均匀混合4AlO2-+7H++H2O→3Al(OH)3↓+Al3+ |
下列有关中和热测定实验说法正确的是( )
| A、中和热测定实验中可以用环形铁丝搅拌棒比环形玻璃搅拌棒更方便 |
| B、中和热测定实验中若将50mL 0.50mol/L盐酸和50mL 0.55mol/L NaOH溶液改为100mL 0.50mol/L盐酸和100mL 0.55mol/L NaOH溶液,所测中和热数值将变为原实验的2倍 |
| C、教材中和热测定实验中所取NaOH的物质的量稍大于HCl,会导致所测中和热数值偏高 |
| D、做1次完整的中和热测定实验,温度计需使用3次 |
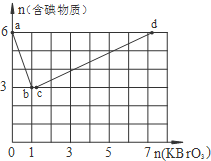 在稀硫酸酸化的含6mol KI溶液中逐滴加入KBrO3溶液,整个过程中含碘物质与所加入KBrO3物质的量的关系如图.请回答下列问题:
在稀硫酸酸化的含6mol KI溶液中逐滴加入KBrO3溶液,整个过程中含碘物质与所加入KBrO3物质的量的关系如图.请回答下列问题: