题目内容
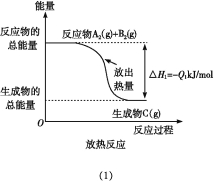
【题目】右图为氯化钠的晶体结构模型,下列说法不正确的是
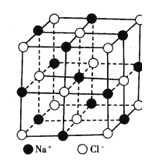
A.NaC1晶体中Na+与C1— 的个数比为1:1
B.每个Na+周围距离最近的C1— 数为6
C.和Na+距离相等且最近的C1— 构成的多面体是正八面体
D.每个Na+周围距离最近的Na+数为8
【答案】D
【解析】
试题分析:A.根据图示NaCl晶胞,Na+个数是:1/8×8+1/2×6=4,Cl-个数是:12×1/4+1=4,则NaC1晶体中Na+与C1— 的个数比为1:1,A项正确;B.每个Na+周围距离最近的C1— 数为6(上、下、左、右、前、后),B项正确;C.由图中心的Cl-与其距离最近的Na+构成的多面体是八面体,C项正确;D.据图可知每个Na+周围距离最近的Na+数为12,D项错误;答案选D。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目