题目内容
已知33As、34Se、35Br位于同一周期,下列关系正确的是
| A.电负性:As>Cl>P | B.热稳定性:HCl>HBr>AsH3 |
| C.第一电离能:Br>Se>As | D.酸性:H3AsO4>H2SO4>H3PO4 |
B
解析试题分析:A、电负性: Cl>P>As,错误;B、非金属性决定气态氢化物的热稳定性:HCl>HBr>AsH3,正确;C、第一电离能应为:Br>As >Se,错误。D、非金属性决定酸性: H2SO4>H3PO4>H3AsO4,错误。
考点:考察元非金属性、电离能、电负性知识。

练习册系列答案
相关题目
某元素X的逐级电离能如图所示,下列说法正确的是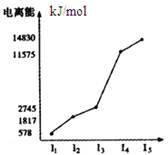
| A.X元素显+4价 |
| B.X为非金属 |
| C.X为第五周期元素 |
| D.X与氯反应时最可能生成的阳离子为X3+ |
下列递变规律正确的是( )
| A.Na、Mg、Al的金属性依次减弱 |
| B.P、S、Cl元素的最高正价依次降低 |
C.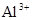 、 、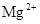 、 、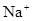 的离子半径依次减小 的离子半径依次减小 |
| D.HNO3、H3PO4、H2SO4酸性依次增强 |
已知X+、Y2+、Z-、W2-四种离子均具有相同的电子层结构。下列关于X、Y、Z、W四种元素的描述,正确的是 ( )
| A.原子半径:X>Y>Z>W |
| B.原子序数:Y>X>Z>W |
| C.原子最外层电子数:Y>X>Z>W |
| D.金属性:X<Y,还原性:W2->Z- |
短周期元素X、Y、z、W的原子序数依次增大,x原子最外层电子数是其内层电子总数的3倍,Y原子最外层只有2个,Z的氧化物可做光纤电缆材料,W与X属于同一主族。下列叙述正确的是( )
| A.元素W的氢化物的热稳定性比X弱,因为X的氢化物分子间存在氢键 |
| B.四种元素形成的最高价氧化物对应水化物的酸性最强的是W |
| C.他合物YX、ZX2、WX3中化学键类型相同 |
| D.原子半径的大小顺序:r(Y)>r(Z)>r(X)>r(W) |
元素性质的周期性变化不包括
| A.原子半径 | B.元素的主要化合价 |
| C.原子核外电子结构 | D.金属性和非金属性 |
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质是一种重要的半导体材料。下列说法中,正确的是( )
| A.X、Y、Z、W的原子半径和原子序数都依次增大 |
| B.W、Z、M元素的气态氢化物热稳定性依次增强 |
| C.M分别和Y、Z所形成化合物都可以和碱反应 |
| D.X分别和M、W所形成的化合物含化学键类型一定相同 |
下列粒子的个数之比不是1∶1的是
| A.氘原子中的质子和中子 |
| B.C2H4分子中的质子和电子 |
| C.Na2O2固体中的阴离子和阳离子 |
| D.常温下,pH=7的CH3COOH与CH3COONa混合溶液中的H+与OH- |
工业上常利用液晶显示屏生产过程中产生的废玻璃粉末为原料回收金属铈(Ce),金属铈是一种重要的稀土元素,原子序数为58,它有四种同位素,元素的相对原子质量为140,下列有关说法正确的是
| A.它是第五周期元素 |
| B.原子核内一定有82个中子 |
| C.铈的四种同位素形成的中性原子核外电子数相同 |
| D.Ce2+离子中有55个质子 |