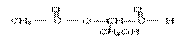��Ŀ����
��֪X��Y��Z��W���ֶ�����Ԫ�ص�ԭ�Ӱ뾶���μ�С�������ڱ���X��Y��Y��Z��λͬһ���ڵ�����λ�ã�X������������Ϊ������������2����W�ֱ�����X��Y��Z��һ��ԭ�������γɵ�������Ϊ10�ij�����������ж�X��Y��Z��W����Ԫ�ز��ش��������⣺��Ҫ����ȷ�����Ԫ�ط��ż��йػ�ѧ�����ʾ��
��1����XY��2����������ԭ������㶼����8���ӣ���д����ṹʽ��______����XY��2����W2��������WXY����ˮ��Һ��һ���ᣬijŨ�ȸ���ļ��Σ�KXY����Һ��ʹ��̪��Һ�Ժ�ɫ���������ӷ���ʽ��ʾ��ԭ��______��
��2����֪��Ȳ��һ�������¿����������ɱ���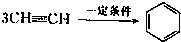 �����谷Ҳ�������谷��WXY�����е�Wԭ�ӱ�����ȡ����ɵ��谷��������������Ȳ�����۷�Ӧ���õ��������谷���Ǽ��Լ�������������������д�������谷�ṹ��ʽ��______��
�����谷Ҳ�������谷��WXY�����е�Wԭ�ӱ�����ȡ����ɵ��谷��������������Ȳ�����۷�Ӧ���õ��������谷���Ǽ��Լ�������������������д�������谷�ṹ��ʽ��______��
��3�������谷��ǿ����ǿ��ˮ��Һ����ˮ�⣬�������ǻ�ȡ�������������ᣮ�����谷���ں������߶���һЩ�̷۳��ҷǷ������̷�����������Ʒ�ĺ��������׳Ƶ����������о����������谷��������������ϸ���н�ϳ����Ӷ��γ�����ʯ��������С�ܣ����������˥�ߣ�������Σ����������д�������谷������������Ļ�ѧ����ʽ��______��
��4����̼�������Ե��ܺġ�����Ⱦ�����ŷ�Ϊ�����ľ���ģʽ������һ�ּ����ǽ�XZ2ת�����л���ʵ��̼ѭ�����磺2XZ2��g��+2W2Z��l���TX2W4��g��+3Z2��g����H=+1411.0kJ/mol��2XZ2��g��+3W2Z��l���TX2W5ZW��l��+3Z2��g����H=+1366.8kJ/mol����X2W4ˮ����X2W5ZW��Ӧ���Ȼ�ѧ����ʽΪ______��
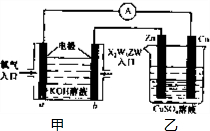
��5������X2W5ZWȼ�ϵ�������ͼ��ʾ��װ�ã�
�����װ����Cu��Ϊ______����
��д��b���ĵ缫��ӦʽΪ______��
�۵�ͭƬ�������仯Ϊ12.8gʱ��a�������ĵ�O2�ڱ�״���µ����Ϊ______L���ס�����װ���е������ҺpH�ı仯Ϊ��______����______����������С���������䡱����
��1����XY��2����������ԭ������㶼����8���ӣ���д����ṹʽ��______����XY��2����W2��������WXY����ˮ��Һ��һ���ᣬijŨ�ȸ���ļ��Σ�KXY����Һ��ʹ��̪��Һ�Ժ�ɫ���������ӷ���ʽ��ʾ��ԭ��______��
��2����֪��Ȳ��һ�������¿����������ɱ���
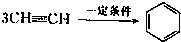 �����谷Ҳ�������谷��WXY�����е�Wԭ�ӱ�����ȡ����ɵ��谷��������������Ȳ�����۷�Ӧ���õ��������谷���Ǽ��Լ�������������������д�������谷�ṹ��ʽ��______��
�����谷Ҳ�������谷��WXY�����е�Wԭ�ӱ�����ȡ����ɵ��谷��������������Ȳ�����۷�Ӧ���õ��������谷���Ǽ��Լ�������������������д�������谷�ṹ��ʽ��______����3�������谷��ǿ����ǿ��ˮ��Һ����ˮ�⣬�������ǻ�ȡ�������������ᣮ�����谷���ں������߶���һЩ�̷۳��ҷǷ������̷�����������Ʒ�ĺ��������׳Ƶ����������о����������谷��������������ϸ���н�ϳ����Ӷ��γ�����ʯ��������С�ܣ����������˥�ߣ�������Σ����������д�������谷������������Ļ�ѧ����ʽ��______��
��4����̼�������Ե��ܺġ�����Ⱦ�����ŷ�Ϊ�����ľ���ģʽ������һ�ּ����ǽ�XZ2ת�����л���ʵ��̼ѭ�����磺2XZ2��g��+2W2Z��l���TX2W4��g��+3Z2��g����H=+1411.0kJ/mol��2XZ2��g��+3W2Z��l���TX2W5ZW��l��+3Z2��g����H=+1366.8kJ/mol����X2W4ˮ����X2W5ZW��Ӧ���Ȼ�ѧ����ʽΪ______��
��5������X2W5ZWȼ�ϵ�������ͼ��ʾ��װ�ã�
�����װ����Cu��Ϊ______����
��д��b���ĵ缫��ӦʽΪ______��
�۵�ͭƬ�������仯Ϊ12.8gʱ��a�������ĵ�O2�ڱ�״���µ����Ϊ______L���ס�����װ���е������ҺpH�ı仯Ϊ��______����______����������С���������䡱����

X��Y��Z��W���ֶ�����Ԫ�ص�ԭ�Ӱ뾶���μ�С��X������������Ϊ������������2����Xԭ��ֻ����2�����Ӳ㣬����������Ϊ4����XΪCԪ�أ�W�ֱ�����X��Y��Z��һ��ԭ�������γɵ�������Ϊ10�ij������������֪WΪHԪ�أ������ڱ���X��Y��Y��Z��λͬһ���ڵ�����λ�ã����ԭ�Ӱ뾶��֪��YΪNԪ�ء�ZΪ��Ԫ�أ�
��1����CN��2����������ԭ������㶼����8���ӣ�Cԭ����Nԭ��֮���γ�3�Թ��õ��Ӷԣ�Cԭ��֮���γ�1�Թ��õ��Ӷԣ���ṹʽΪ��N��C-C��N��
KCN��Һ��ʹ��̪��Һ�Ժ�ɫ��CN-����ˮ��CN-+H2O?HCN+OH-���ƻ�ˮ�ĵ���ƽ�⣬����Һ�ʼ��ԣ�ʹ��̪��Һ�Ժ�ɫ��
�ʴ�Ϊ��N��C-C��N��CN-+H2O?HCN+OH-��
��2�������谷��N��C-NH2���۵õ��������谷���Ǽ��Լ���N��C-NH2��C��N��������һ��C-N�����ѣ�Cԭ����Nԭ�ӽ��������γɣ��������谷�Ľṹ��ʽΪ��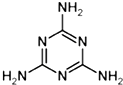 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��3��C3H6N6ˮ���������������һ��������������������ᣬˮ�ⷴӦΪC3H6N6+3H2O=C3N3��OH��3+3NH3���ʴ�Ϊ��C3H6N6+3H2O=C3N3��OH��3+3NH3��
��4����֪���١�2CO2��g��+2H2O��l���TC2H4��g��+3O2��g����H=+1411.0kJ/mol��
�ڡ�2CO2��g��+3H2O��l���TC2H5OH��l��+3O2��g����H=+1366.8kJ/mol��
���ݸ�˹���ɣ���-�ٵ�C2H4��g��+H2O��l���TC2H5OH��l����H=-44.2kJ/mol��
�ʴ�Ϊ��C2H4��g��+H2O��l���TC2H5OH��l����H=-44.2kJ/mol��
��5����ԭ�������������ԭ��Ӧ����������������Ӧ��C2H5OHȼ�ϵ��������������ͨ�롢�Ҵ��ڸ������룬��C2H5OHȼ�ϵ��װ��ͼ��֪��aΪԭ���������bΪԭ��ظ������ұ�װ��Ϊ��Ƴأ�Cu����ԭ���������Ϊ�������ʴ�Ϊ������
��bΪԭ��ظ������Ҵ�ʧȥ���ӣ���������������̼�����ˮ��b���ĵ缫��ӦʽΪ��C2H5OH+16OH--12e-=2CO32-+11H2O��
�ʴ�Ϊ��C2H5OH+16OH--12e-=2CO32-+11H2O��
�۵�ͭƬ�������仯Ϊ12.8gʱ�������ʵ���=
=0.2mol��Cu�缫��Ӧʽ��Cu-2e-=Cu2+����ת�Ƶ������ʵ���=0.2mol��2=0.4mol�����ݵ���ת���غ��֪��a�������ĵ�O2�����ʵ���=
=0.1mol���ʱ�����������������Ϊ0.1mol��22.4L/mol=2.24L��
ԭ����ܷ�Ӧʵ��Ϊ���Ҵ�ȼ�����ɶ�����̼��ˮ��������̼�����������Ʒ�Ӧ����̼������ˮ��NaOH��Ũ�ȼ��ͣ���Һ���Լ������ʼ�װ������ҺpH��С��
�ұ�װ��Ϊ��Ƴأ�Cu����ԭ���������Ϊ������Zn����ԭ��ظ�����Ϊ�����������缫��ӦʽΪ��Cu-2e-=Cu2+�������缫��ӦʽΪ��Cu2++2e-=Cu���������Һ��Ũ�Ȳ��䣬����װ������ҺpH���䣬
�ʴ�Ϊ����С�����䣮
��1����CN��2����������ԭ������㶼����8���ӣ�Cԭ����Nԭ��֮���γ�3�Թ��õ��Ӷԣ�Cԭ��֮���γ�1�Թ��õ��Ӷԣ���ṹʽΪ��N��C-C��N��
KCN��Һ��ʹ��̪��Һ�Ժ�ɫ��CN-����ˮ��CN-+H2O?HCN+OH-���ƻ�ˮ�ĵ���ƽ�⣬����Һ�ʼ��ԣ�ʹ��̪��Һ�Ժ�ɫ��
�ʴ�Ϊ��N��C-C��N��CN-+H2O?HCN+OH-��
��2�������谷��N��C-NH2���۵õ��������谷���Ǽ��Լ���N��C-NH2��C��N��������һ��C-N�����ѣ�Cԭ����Nԭ�ӽ��������γɣ��������谷�Ľṹ��ʽΪ��
 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
����3��C3H6N6ˮ���������������һ��������������������ᣬˮ�ⷴӦΪC3H6N6+3H2O=C3N3��OH��3+3NH3���ʴ�Ϊ��C3H6N6+3H2O=C3N3��OH��3+3NH3��
��4����֪���١�2CO2��g��+2H2O��l���TC2H4��g��+3O2��g����H=+1411.0kJ/mol��
�ڡ�2CO2��g��+3H2O��l���TC2H5OH��l��+3O2��g����H=+1366.8kJ/mol��
���ݸ�˹���ɣ���-�ٵ�C2H4��g��+H2O��l���TC2H5OH��l����H=-44.2kJ/mol��
�ʴ�Ϊ��C2H4��g��+H2O��l���TC2H5OH��l����H=-44.2kJ/mol��
��5����ԭ�������������ԭ��Ӧ����������������Ӧ��C2H5OHȼ�ϵ��������������ͨ�롢�Ҵ��ڸ������룬��C2H5OHȼ�ϵ��װ��ͼ��֪��aΪԭ���������bΪԭ��ظ������ұ�װ��Ϊ��Ƴأ�Cu����ԭ���������Ϊ�������ʴ�Ϊ������
��bΪԭ��ظ������Ҵ�ʧȥ���ӣ���������������̼�����ˮ��b���ĵ缫��ӦʽΪ��C2H5OH+16OH--12e-=2CO32-+11H2O��
�ʴ�Ϊ��C2H5OH+16OH--12e-=2CO32-+11H2O��
�۵�ͭƬ�������仯Ϊ12.8gʱ�������ʵ���=
| 12.8g |
| 64g/mol |
| 0.4mol |
| 4 |
ԭ����ܷ�Ӧʵ��Ϊ���Ҵ�ȼ�����ɶ�����̼��ˮ��������̼�����������Ʒ�Ӧ����̼������ˮ��NaOH��Ũ�ȼ��ͣ���Һ���Լ������ʼ�װ������ҺpH��С��
�ұ�װ��Ϊ��Ƴأ�Cu����ԭ���������Ϊ������Zn����ԭ��ظ�����Ϊ�����������缫��ӦʽΪ��Cu-2e-=Cu2+�������缫��ӦʽΪ��Cu2++2e-=Cu���������Һ��Ũ�Ȳ��䣬����װ������ҺpH���䣬
�ʴ�Ϊ����С�����䣮

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ