题目内容
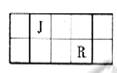
(7分)J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的元素。
(1)元素T在周期表中的位置是位于①_________。
(2)J和氢组成的化合物A每个分子由4个原子组成且含有2个氢原子,其结构式为②________________,已知充分燃烧a gA物质时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则A物质燃烧热的热化学方程式是③__________。
(3)M和R形成的一种化合物能使酸性高锰酸钾溶液褪色,该反应的离子方程式为④______________。
(4)在微电子工业中,L的最简单气态氢化物的水溶液可作刻蚀剂H2O2 的清除剂,所发生反应的产物不污染环境,其化学方程式为:⑤ 。
(5)写出三种仅由上述五种元素中的一种或两种元素形成的漂白剂的化学式:⑥ __________________。
(6)其中L、M、R形成的氢化物沸点由高到低的顺序是⑦ (用化学式表示)
(1)第三正确第ⅦA 族。
(2) CH≡CH ;C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l); ΔH=-2b kJ / mol
(3)2MnO4ˉ + 5SO2 + 2H2O = 2Mn2+ +5SO42- + 4H+
(4)2NH3 + 3H2O2 = N2 + 6H2O _。
(5) O3、Cl2、SO2、ClO2 任写三个
(6) H2O> NH3> H2S
【解析】考查元素周期表的结构及其应用。
地壳中含量最多的元素是氧,则M是氧。J元素最低负化合价的绝对值与其原子最外层电子数相等,则J是第ⅣA元素,根据J的物质可判断J是碳,则R是硫。由于原子序数依次增大,所以L是N,T是Cl。
(2)含有2个氢原子的有机物是乙炔,结构式为CH≡CH。燃烧热是指在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物所放出的热量,生成1mol二氧化碳气体,放出热量是b kJ,所以燃烧热多的热化学方程式为C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l); ΔH=-2b kJ / mol。
(3)能使酸性高锰酸钾溶液褪色,说明该化合物具有还原性,因此是SO2,方程式为2MnO4ˉ + 5SO2 + 2H2O = 2Mn2+ +5SO42- + 4H+。
(4)氮的氢化物是氨气,具有还原性,被双氧水氧化生成氮气和水,方程式为2NH3 + 3H2O2 = N2 + 6H2O。
(5)常见漂白剂有O3、Cl2、SO2、ClO2等。
(6)水和氨气中都存在氢键,但氧原子的非金属性强于氮原子的,所以形成的氢键要,常温下是液体,氨气是气体,所以沸点高低顺序为H2O> NH3> H2S。

 黄冈创优卷系列答案
黄冈创优卷系列答案 (2010?福建)J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素.
(2010?福建)J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素.
 Al(OH)3+3HCl
Al(OH)3+3HCl
 J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素.
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素.
 J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素.
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如表;J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素.