题目内容
14.下列各组元素性质递变规律不正确的是( )| A. | N、O、F原子半径依次增大 | |
| B. | P、S、Cl元素最高化合价依次增高 | |
| C. | Li、Be、B三种元素的原子随着原子序数的增加最外层电子数依次增多 | |
| D. | Na、K、Rb的金属性依次增强 |
分析 A.同周期自左而右原子半径减小;
B.第三周期自左而右主族元素最高正化合价依次增大;
C.同周期自左而右最外层电子数依次增大;
D.同主族自上而下金属性增强.
解答 解:A.N、O、F同周期,核电荷数依次增大,原子半径依次减小,故A错误;
B.P、S、Cl元素最高化合价依次为+5、+6、+7,故B正确;
C.Li、Be、B三种元素的原子随着原子序数依次增加,最外层电子数依次为1、2、3,故C正确;
D.同主族自上而下金属性增强,故Na、K、Rb的金属性依次增强,故D正确,
故选A.
点评 本题考查元素周期律,比较基础,侧重考查学生对元素周期律的理解掌握,有利于基础知识的巩固.

练习册系列答案
相关题目
4.下列各物质中的少量杂质,可用括号内的试剂和方法除去的是( )
| A. | 乙醇中含有水(生石灰,蒸馏) | |
| B. | 甲烷中含有乙烯(溴水,洗气) | |
| C. | 溴苯中溶有溴(苯,分液) | |
| D. | 乙烷中含有乙烯(酸性高锰酸钾溶液,洗气) |
5.将0.1mol N2和0.3mol H2置于密闭容器中发生反应:N2+3H2?2NH3,下列关于该反应的说法中正确的是( )
| A. | 增大压强,反应速率减小 | |
| B. | 最终可生成0.2 mol NH3 | |
| C. | 升髙温度,反应速率增大 | |
| D. | 当V正(N2):V 正(H2)=1:3时,一定达化学平衡状态 |
2.下列关于化学反应限度的叙述错误的是( )
| A. | 不同的化学反应,限度可能不同 | |
| B. | 可以通过改变温度来控制化学反应的限度 | |
| C. | 可以通过延长化学反应的时间来改变化学反应的限度 | |
| D. | 一个化学反应在一定条件下达到限度时,正、逆反应速率相等 |
9.已知,SO2气体和Cl2均具有漂白性,二者能发生反应如下:Cl2+SO2+2H2O=H2SO4+2HCl.下列叙述正确的是( )
| A. | 将等物质的量的SO2气体和Cl2同时作用于湿润的红色布条,漂白效果将更好 | |
| B. | SO2气体和Cl2 漂白原理相同 | |
| C. | SO2气体和Cl2均是有毒气体 | |
| D. | SO2只有氧化性没有还原性 |
19.主族元素X的阳离子和主族元素Y的阴离子具有与氩原子相同的电子层结构,下列叙述正确的是( )
| A. | X的原子半径比Y的大 | B. | X原子的最外层电子数比Y的大 | ||
| C. | X的原子序数比Y的小 | D. | X元素的最高正价比Y的大 |
6.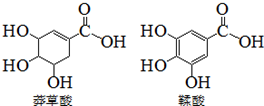 莽草酸是一种合成药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )
莽草酸是一种合成药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )
 莽草酸是一种合成药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )
莽草酸是一种合成药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.下列关于这两种有机化合物的说法正确的是( )| A. | 两种酸遇三氯化铁溶液都显色 | |
| B. | 鞣酸分子比莽草酸分子多两个双键 | |
| C. | 等物质的量的两种酸与NaOH反应,消耗NaOH的量相同 | |
| D. | 两种酸都能与溴水反应 |
3.下列关于有机物的不正确说法是( )
| A. | 油脂是产生能量最高的营养物质 | |
| B. | 苯能发生氧化反应 | |
| C. | 纤维素可在人体内最终水解成葡萄糖 | |
| D. | 谷氨酸分子中含有2种官能团 |