题目内容
【题目】水溶液中能大量共存的一组离子是( )
A.K+、Al3+、NO3﹣、ALO2﹣
B.H+、Na+、Fe2+、ClO﹣
C.Na+、Ba2+、Cl﹣、NO3﹣
D.K+、NH4+、CO32﹣、OH﹣
【答案】C
【解析】解:A.Al3+、AlO2﹣之间发生双水解反应生成氢氧化铝沉淀,在溶液中不能大量共存,故A错误;
B.H+、Fe2+与ClO﹣发生反应,在溶液中不能大量共存,故B错误;
C.Na+、Ba2+、Cl﹣、NO3﹣之间不发生反应,在溶液中能够大量共存,故C正确;
D.NH4+、OH﹣之间发生反应,在溶液中不能大量共存,故D错误;
故选C.

【题目】A、B、C、D、E为原子序数依次增大的短周期主族元素,其原子半径与最外层电子数的关系如下图1。E原子最外层上的电子数是D原子最外层电子数的4倍,D离子核外电子排布与C2-相同。
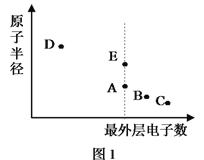
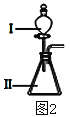
试回答:
(1)元素E在元素周期表中的位置是___________________。
(2)与元素D离子所含电子数和质子数均相同的微粒是________________。(用化学式作答,下同)
(3)B和E最高价氧化物对应的水化物,酸性较弱的_________________。若用上图2中装置验证这两种酸的酸性强弱,则在装置中加入的试剂分别为:Ⅰ___________,Ⅱ__________,观察到的实验现象是________________________。
(4)由以上五种元素组成的物质,其组成和结构信息如下表:
物质 | 组成和结构信息 |
a | 含有A、C、D的盐 |
b | C、D组成的化合物,且原子数之比为1∶1 |
c | 化学组成为AC2 |
①a含有的化学键有___________________________________;
②b与c反应的化学方程式为_________________________________。